慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)是一种常见的以持续性呼吸系统症状和气流受限为特征的疾病[1]。目前研究证实,COPD的发生发展与免疫失衡密切相关,而辅助性T细胞/调节性T细胞(Th17/Treg)的失衡在其中起着重要作用[2]。COPD属于中医学“肺胀”范畴,是由于慢性肺系疾病日久导致肺脾肾虚损,形成痰、饮、瘀等病理产物所致[3]。虚实夹杂、正虚积损为COPD的主要病机,其中肺脾气虚贯穿肺胀的全过程[4],且肺脾气虚证是肺胀的常见证型[5]。升阳益胃汤首载于李杲《内外伤辨惑论》,是肺脾同治的经典代表方剂。目前,关于升阳益胃汤有效治疗COPD的临床观察文献[6-8]较多,但其作用机制研究尚欠缺。本研究从免疫失衡角度观察升阳益胃汤对COPD肺脾气虚证模型大鼠肺组织、胃肠组织病理改变的影响并探讨其可能的作用机制。本实验方案经贵州中医药大学动物实验中心批准(伦理批准号:20210059)。
1 材料及方法
1.1 动物
SPF级SD雄性大鼠84只,体质量(200±20)g,4~5周龄,购于湖南省长沙市天勤生物技术有限公司,实验动物生产许可证号:SCXK(湘)2019-0014。饲料均为普通级饲料,饲养温度25 ℃、湿度80%,自由进食饮水。
1.2 药物
升阳益胃汤组成:黄芪30 g,法半夏15 g,人参15 g,炙甘草15 g,独活9 g,防风9 g,白芍9 g,羌活9 g,陈皮6 g,茯苓5 g,北柴胡5 g,泽泻5 g,白术5 g,黄连1.5 g。饮片煎煮前加10倍量蒸馏水浸泡30 min,按常规煎药法煎煮2次,每次30 min,过滤药液并浓缩至1 ml药液含生药2 g,经高压灭菌冷却,4 ℃冰箱保存备用。大黄1000 g(同济堂中药智能免煎颗粒剂),按药物︰水=1︰1方法配置成混悬液,浓度为l g/ml。醋酸地塞米松片(新乡市常乐制药有限公司,批号:1907066,0.75 mg/片),配置成浓度为0.00675 g/ml溶液。瑞巴派特片(浙江远力健药业有限责任公司,批号:21111402,0.1 g/片),配置成浓度为0.009 g/ml溶液。
1.3 主要试剂及仪器
遵义牌香烟(焦油量10 mg,烟气烟碱量0.8 mg,烟气一氧化碳量12 mg,批号:208041899891607),贵州中烟工业有限责任公司;脂多糖(LPS,批号:0000097034),上海尤宁维生物科技股份有限公司;HE染色液(批号:H8070),北京赛因坦科技有限公司;髓过氧化物酶(MPO,批号:R4G85ERJ3C)、二胺氧化酶(DAO,批号:20210320)试剂盒,钰博生物科技有限公司;白细胞介素6(IL-6,批号:70-EK306/3-48)、白细胞介素10(IL-10,货号:EK0418)、白细胞介素17(IL-17,批号:A382110145)、转化生长因子β(TGF-β,货号:20r6523)ELISA试剂盒,上海江莱生物科技有限公司;SYBRGreen PCR试剂盒(货号:F-415XL)、逆转录试剂盒(货号:K1622),Thermo公司;水合氯醛(批号:EB05980)、多聚甲醛(货号:ST1127),上海士锋生物科技有限公司;红细胞裂解液(货号:349202),Becton Dickinson公司。
多功能酶标仪(型号:Thermo Multiskan™ FC)、Real-time检测仪(型号:ABI-7500),赛默飞世尔科技(中国)有限公司;台式离心机(型号:NX-1),北京鼎昊源科技有限公司;电热恒温干燥箱(型号:GZX-DH-50x55),上海跃进医疗器械厂;组织脱水机(型号:JJ-12J),武汉俊杰电子有限公司;电子分析天平(型号:FA2004),上海舜宇恒平科学仪器有限公司;组织切片机(型号:RM2235),北京昊诺斯科技有限公司;低温冷冻离心机(型号:5417R),德国艾本德股份公司;光学显微镜(型号:XDS-1A)、倒置显微镜(型号:IX71),OLYMPUS公司;流式细胞仪(型号:beckmancoulter CytoFLEX),BD-FACSVerse公司。
1.4 分组及造模
将84只SD大鼠适应性喂养1周以后,采用随机数字表法分为空白组、模型组、瑞巴派特组、地塞米松组和升阳益胃汤高、中、低剂量组,每组12只。除空白组外,其余各组大鼠采用香烟烟熏+ LPS气管内滴注[9]的方法建立COPD大鼠模型:大鼠在封闭的笼子(1 m×1 m×1 m)里进行每日1 h 10根香烟烟熏,连续28天;在造模的第1天及第14天予10%水合氯醛(0.3 ml/100 g)腹腔麻醉,将麻醉后的大鼠呈仰卧位的姿势固定于鼠板,照射大鼠的喉部,充分暴露声门,将一次性的套针在光源的照射下迅速插入大鼠气管内,拔出套管内的钢芯,以棉丝放于套针外观察是否随大鼠呼吸有规律地波动,插管成功后予1 ml注射器先抽取0.3 ml的空气再抽取0.2 ml(0.2 mg)LPS推入气管内,完成后将大鼠直立反复旋转摇晃1~2 min,使LPS充分均匀分布于双肺。空白组用一次性气管插管法予0.2 ml生理盐水支气管滴药。从熏烟后第8天开始,除空白组外其他各组大鼠以苦寒泻下法[10]建立肺脾气虚证模型,即给予大黄混悬液1 ml/100 g灌胃,每日1次,连续给药8天,空白组大鼠给予生理盐水1 ml/100 g灌胃。
1.5 给药方法
造模第15天,参照大鼠体表面积与人体体表面积的换算公式[11]换算给药剂量,升阳益胃汤中剂量组为人临床等效剂量。升阳益胃汤高、中、低剂量组大鼠分别给予升阳益胃汤24.930、12.465、6.233 g/(kg·d)灌胃,地塞米松组给予醋酸地塞米松片溶液0.0675 mg/(kg·d)灌胃,瑞巴派特组给予瑞巴派特片溶液9 mg/(kg·d)灌胃,空白组、模型组给予生理盐水10 ml/(kg·d)灌胃。各组均每日灌胃1次,连续14天。
1.6 观察指标及方法
1.6.1 大鼠的一般情况
实验期间采用24 h活动录像观察各组大鼠精神活动、皮毛光泽、饮食及大小便情况,并记录各组大鼠体质量。
1.6.2 肺、气管、胃、小肠组织病理观察
实验第31天将大鼠禁食24 h,然后予10%水合氯醛腹腔麻醉(0.3 ml/100 g)进行腹主动脉取血,摘取左肺上叶、气管、胃、小肠组织,经4%的多聚甲醛固定24 h脱水,将组织透明、浸蜡、包埋、切片,HE染色,中性树胶封固,晾干后在光学显微镜下进行病理观察。
1.6.3 外周血Th17、Treg水平及Th17/Treg值
收集大鼠外周血于抗凝管中,加入4倍体积的红细胞裂解液充分裂解后,于离心机1000 r/min(离心半径4.5 cm)、37 ℃离心8 min;去上清,用PBS清洗细胞沉淀3次;以1︰100的稀释比例孵育抗体30 min;调整细胞密度,过筛网,采用流式细胞术测定Th17、Treg水平,计算Th17/Treg值。具体操作按照试剂盒说明书进行。
1.6.4 血清炎症因子及肺组织MPO水平
大鼠腹主动脉取血,于离心机4000 r/min(离心半径4.5 cm)、37 ℃离心10 min,取上清备用。ELISA法检测大鼠血清DAO、IL-6、IL-10、IL-17、TGF-β水平。取出右肺上叶组织放于冻存管内置于冰上待测,检测肺组织MPO水平。具体检测方法按照试剂盒说明书进行。
1.6.5 肺组织叉状头/翅膀状螺旋转录因子(FoxP3)、维甲酸相关核孤儿受体γ(RORγt) mRNA表达
采用实时荧光定量PCR法测定。摘取大鼠右肺下叶组织充分研磨,分别加入Trizol裂解液裂解细胞提取RNA,逆转录cDNA,逆转录条件:42 ℃ 40 min;85 ℃ 5 min。将制备好的cDNA进行PCR扩增,扩增体系如下:SYBRGreen Mix 10 µl,上游引物0.4 µl,下游引物0.4 µl,ddH2O 7.2 µl,cDNA模板2 µl,总体积20 µl。扩增条件:94 ℃ 10 min,(94 ℃ 20 s,55 ℃ 20 s,72 ℃ 20 s)40个循环。数据采用ABI Prism 7500 SDS 软件分析。引物由无锡菩禾生物医药技术有限公司设计,GAPDH:上游ACAGCAACAGGGTGGTGGAC,下游TTTGAGGGTGCAGCGAACTT,252 bp;FoxP3:上游TCTCAAG CACTGCCAAGC,下游TCTCCGCACAGCAAACAA,289 bp;RORγt:上游AAGGCAAATACGGTGGTGT,下游GTAGAGGGCAATCTCATCC,125 bp。采用2-△△CT法分析目的基因的相对表达量。
1.7 统计学方法
采用SPSS 26.0软件与Graphpad Prism 8.0软件进行统计分析与制图。计量资料均符合正态分布以均数±标准差(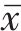
2 结果
2.1 各组大鼠一般情况比较
空白组大鼠精神良好,皮毛光泽,活动自如,饮食正常、每日约进食50 g,大便质软成形、每日1或2次,小便每日3或4次。模型组大鼠精神倦怠,腹背部部分皮毛色泽黯淡发黄,活动减少或喜静卧,进食量每日约15 g,大便多不成形或成稀糊状、每日3~5次,小便量多、每日7或8次,易尿失禁。升阳益胃汤低剂量组大鼠精神欠佳,皮毛色泽黯淡,活动减少,进食量每日约20 g,稀便较多、每日3~5次,小便每日6或7次。升阳益胃汤中剂量组大鼠精神欠佳,皮毛稍有色泽,活动减少,进食量每日30~35 g,大便质软稍成形或伴有稀便、每日2~4次,小便每日5或6次。升阳益胃汤高剂量组大鼠精神稍倦怠,皮毛稍有色泽,活动可,进食量每日35~40 g,大便质软成形、每日1或2次,小便每日3或4次。地塞米松组大鼠精神倦怠,皮毛色泽黯淡,活动减少,进食量每日约20 g,大便时质软、时稀便、每日2或3次,小便每日6或7次。瑞巴派特组大鼠精神稍倦怠,皮毛稍有色泽,活动尚可,进食量每日40~45 g,大便质软成形、每日1或2次,小便每日3或4次。表1示,各组大鼠体质量差异无统计学意义(P>0.05)。
| 组别 | 鼠数 | 体质量 |
|---|---|---|
| 空白组 | 12 | 344.3±10.97 |
| 模型组 | 12 | 358.7±8.02 |
| 地塞米松组 | 12 | 338.7±15.28 |
| 瑞巴派特组 | 12 | 374.7±9.29 |
| 升阳益胃汤低剂量组 | 12 | 334.0±9.85 |
| 升阳益胃汤中剂量组 | 12 | 333.7±17.62 |
| 升阳益胃汤高剂量组 | 12 | 339.0±16.09 |
2.2 各组大鼠肺组织病理学形态比较
图1示,空白组大鼠肺组织肺泡结构完整,肺泡壁正常,血管结构正常,肺泡腔和肺间质无明显炎症细胞渗出,无明显红细胞渗出;模型组肺泡结构不完整,肺泡壁增厚严重,血管内有淤血,部分血管伴有粉染蛋白样物质,肺泡腔和肺间质有大量炎症细胞渗出,有大量红细胞渗出;地塞米松组肺泡结构完整,肺泡壁增厚,血管内有淤血,部分血管伴有粉染蛋白样物质,肺泡腔和肺间质有大量实质结构,无明显红细胞渗出;瑞巴派特组肺泡结构不完整,肺泡壁增宽,极少数血管中含有淤血,肺泡腔和肺间质有大量红细胞渗出;升阳益胃汤低剂量组肺泡结构不完整,部分肺泡壁增厚严重,血管内有淤血,部分血管伴有粉染蛋白样物质,肺泡腔和肺间质有大量炎症细胞渗出,无明显红细胞渗出;升阳益胃汤中剂量组肺泡结构不完整,肺泡壁增厚严重,血管内有淤血,少量血管伴有粉染蛋白样物质,肺泡腔和肺间质有部分炎症细胞渗出,有少量红细胞渗出;升阳益胃汤高剂量组肺泡结构不完整,肺泡壁增厚严重,少量血管内有淤血,少量血管伴有粉染蛋白样物质,肺泡腔和肺间质有部分炎症细胞渗出,有大量红细胞渗出。
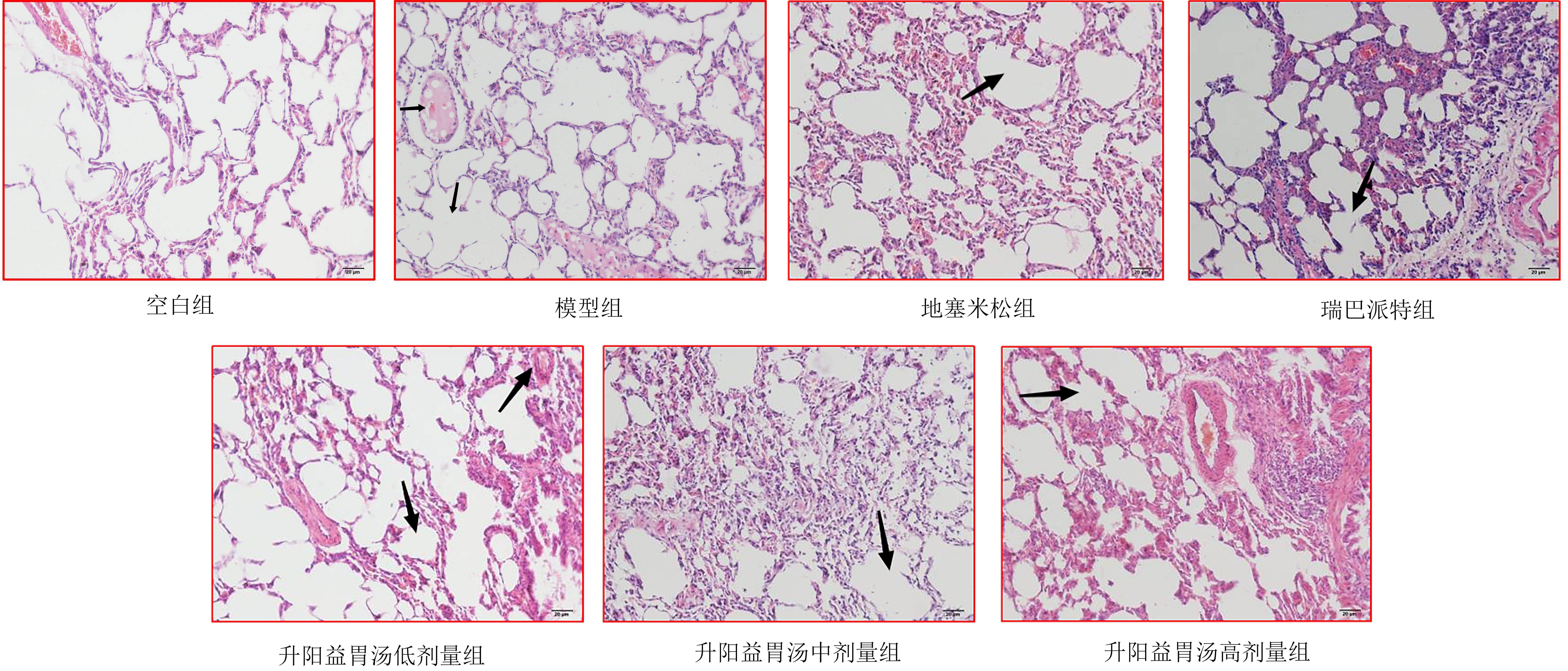
2.3 各组大鼠气管组织病理学形态比较
图2示,空白组大鼠气管组织软骨结构正常,黏膜绒毛排列整齐,无明显上皮细胞脱落;模型组软骨结构正常,黏膜绒毛排列疏松,有少量上皮细胞脱落;地塞米松组软骨结构正常,黏膜绒毛基层细胞增生严重,无明显上皮细胞脱落;瑞巴派特组气管的固有层中可见淋巴细胞,有明显的红细胞,杯状细胞明显增多;升阳益胃汤低剂量组软骨结构正常,黏膜绒毛排列较疏松,有少量上皮细胞脱落;升阳益胃汤中剂量组软骨结构正常,黏膜绒毛排列较疏松,绒毛基层细胞增生略严重,有少量上皮细胞脱落;升阳益胃汤高剂量组软骨结构正常,黏膜绒毛排列较疏松,黏膜绒毛基层细胞增生严重,无明显上皮细胞脱落。
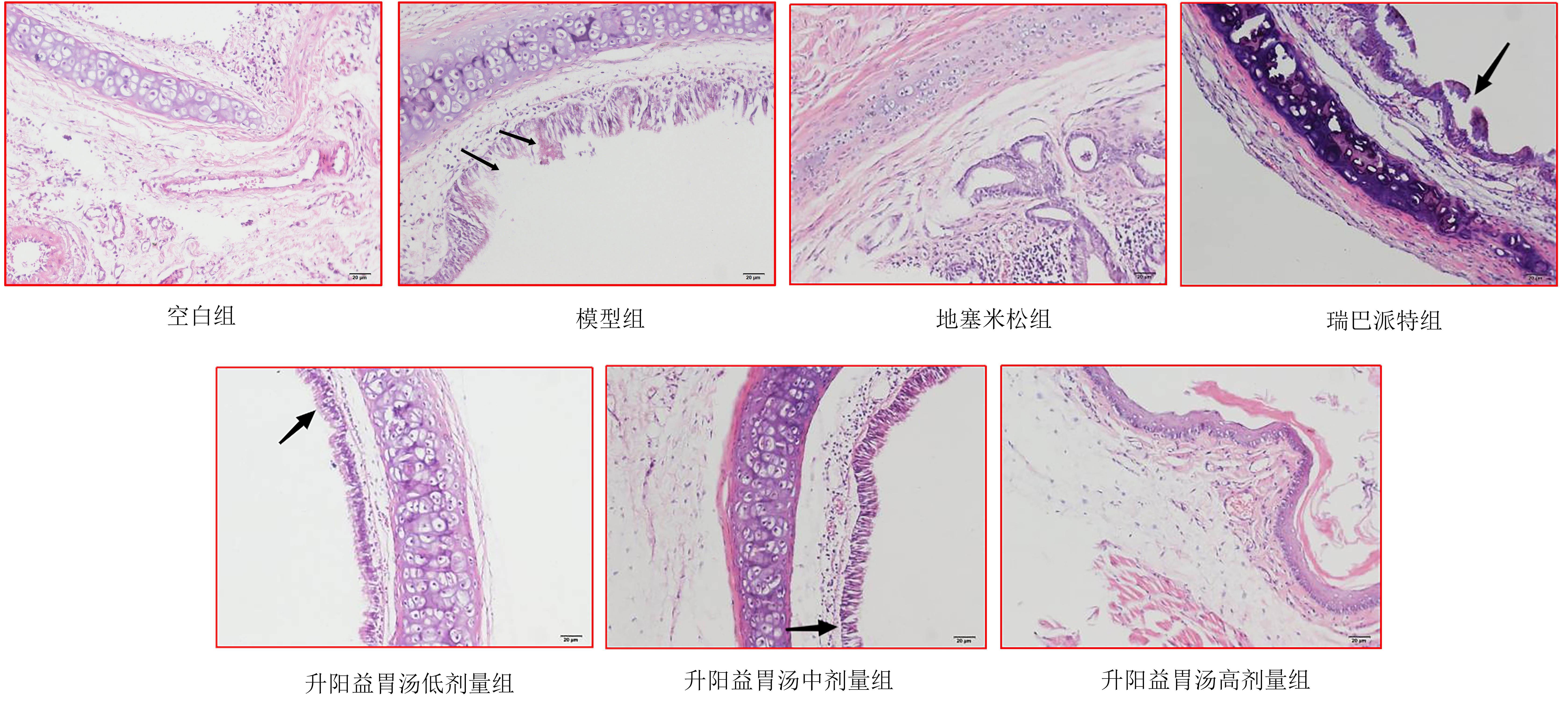
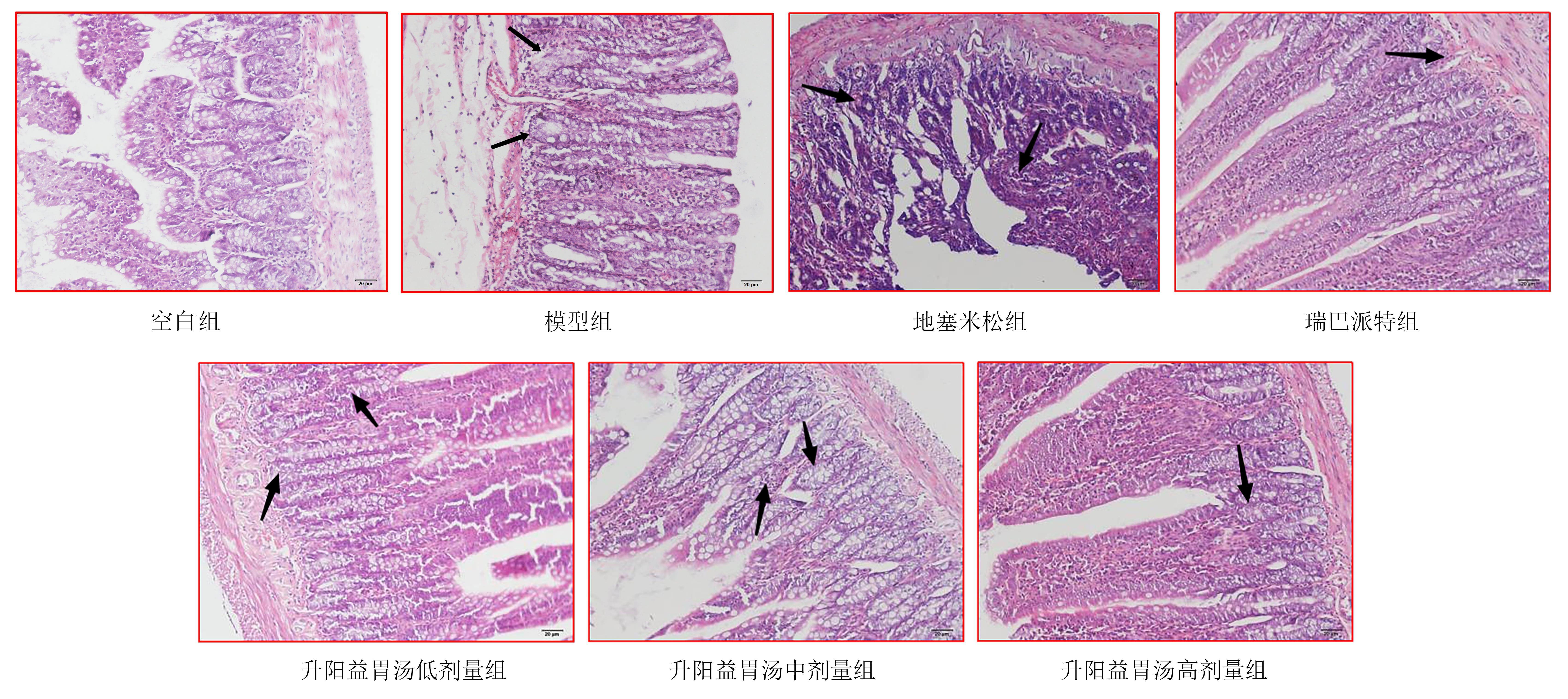
2.4 各组大鼠胃组织病理学形态比较
图3示,空白组大鼠胃黏膜层胃腺排列整齐,无明显红细胞渗出,肌层排列整齐紧密;模型组胃黏膜层胃腺排列紊乱,基质细胞增生严重,有少量红细胞渗出,肌层排列略疏松;地塞米松组胃黏膜层胃腺排列略紊乱,基质细胞少量增生,有极少量红细胞渗出,肌层排列紧密;瑞巴派特组胃黏膜层可见明显的红细胞,胃腺间隙增大、排列疏松;升阳益胃汤低剂量组胃黏膜层胃腺排列紊乱,基质细胞增生严重,有少量红细胞渗出,肌层排列略疏松;升阳益胃汤中剂量组胃黏膜层胃腺排列略紊乱,基质细胞部分增生,有少量红细胞渗出,肌层排列略疏松;升阳益胃汤高剂量组胃黏膜层胃腺排列整齐,基质细胞无明显增生,无明显红细胞渗出,肌层排列紧密。
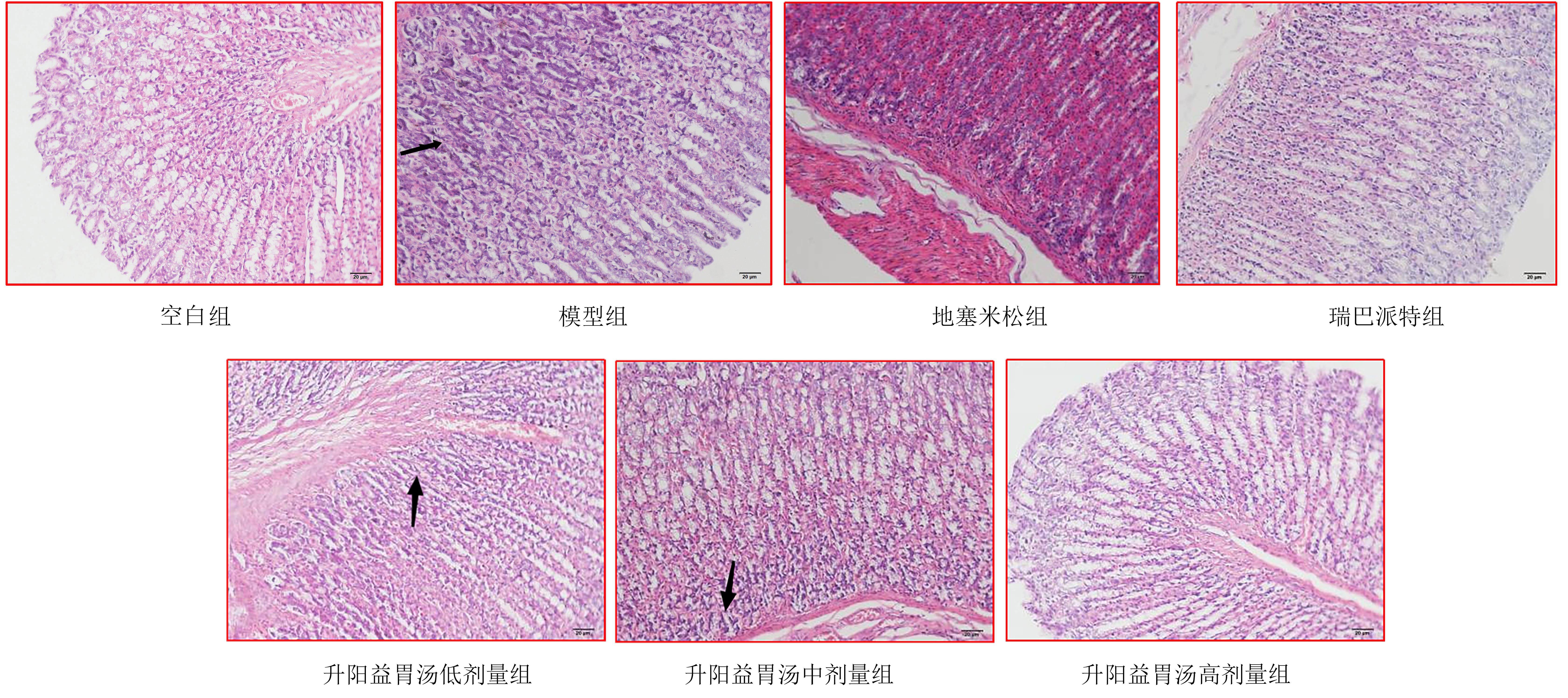
2.5 各组大鼠小肠组织病理学形态比较
图4示,空白组大鼠肠腺数目正常,黏膜层结构完整,黏膜下层排列紧密,未有明显淋巴细胞浸润;模型组肠腺数目减少,黏膜上皮细胞脱落严重,黏膜下层排列疏松,固有层有明显淋巴细胞浸润;地塞米松组肠腺数目略减少,黏膜层结构完整,黏膜下层排列略疏松,有少量淋巴细胞浸润;瑞巴派特组肠腺数目减少,黏膜层排列疏松,结构不完整;升阳益胃汤低剂量组肠腺数目减少,黏膜上皮细胞少量脱落,黏膜下层排列疏松,固有层有明显淋巴细胞浸润;升阳益胃汤中剂量组肠腺数目略减少,黏膜上皮细胞少量脱落,黏膜下层排列较疏松,固有层有明显淋巴细胞浸润;升阳益胃汤高剂量组肠腺数目略减少,黏膜上皮细胞少量脱落,黏膜下层排列较疏松,固有层有少量淋巴细胞浸润。
2.6 各组大鼠外周血Th17、Treg水平及Th17/Treg值比较
表2示,与空白组比较,模型组大鼠外周血Th17水平及Th17/Treg值升高,Treg水平降低(P<0.05);与模型组比较,各药物干预组Th17水平及Th17/Treg值降低,Treg水平升高(P<0.05);与地塞米松组比较,除升阳益胃汤中剂量组Treg水平差异无统计学意义(P>0.05)外,升阳益胃汤各剂量组Th17水平及Th17/Treg值升高,Treg水平降低(P<0.05);与瑞巴派特组比较,升阳益胃汤高剂量组Th17水平及Th17/Treg值降低(P<0.05);与升阳益胃汤低剂量组比较,升阳益胃汤中、高剂量组Th17水平降低,升阳益胃汤高剂量组Th17/Treg值降低(P<0.05);与升阳益胃汤中剂量组比较,升阳益胃汤高剂量组Th17水平及Th17/Treg值降低(P<0.05)。
| 组别 | 鼠数 | Th17 | Treg | Th17/Treg |
|---|---|---|---|---|
| 空白组 | 12 | 0.47±0.13 | 19.20±0.35 | 0.02±0.0068 |
| 模型组 | 12 | 5.81±0.19a) | 12.85±0.64a) | 0.45±0.0274a) |
| 地塞米松组 | 12 | 2.50±0.15b) | 16.02±0.27b) | 0.16±0.0099b) |
| 瑞巴派特组 | 12 | 4.97±0.13b) | 15.54±0.40b) | 0.32±0.0105b) |
| 升阳益胃汤低剂量组 | 12 | 5.28±0.24b)c) | 15.30±0.31b)c) | 0.35±0.0189b)c) |
| 升阳益胃汤中剂量组 | 12 | 4.85±0.25b)c)e) | 15.80±0.26b) | 0.31±0.0179b)c) |
| 升阳益胃汤高剂量组 | 12 | 4.33±0.10b)c)d)e)f) | 15.44±0.24b)c) | 0.28±0.0084b)c)d)e)f) |
2.7 各组大鼠肺组织MPO及血清炎症因子水平比较
表3示,与空白组比较,模型组大鼠肺组织MPO及血清DAO、IL-6、IL-17、TGF-β水平升高,血清IL-10水平降低(P<0.05)。与模型组比较,升阳益胃汤高剂量组、瑞巴派特组及地塞米松组MPO、DAO、IL-6、IL-17、TGF-β水平降低,IL-10水平升高(P<0.05);升阳益胃汤中剂量组TGF-β、IL-6水平降低,IL-10水平升高(P<0.05);升阳益胃汤低剂量组仅TGF-β水平降低(P<0.05)。与地塞米松组比较,瑞巴派特组MPO、TGF-β、DAO水平降低(P<0.05);升阳益胃汤低剂量组TGF-β、IL-6水平升高,IL-10水平降低(P<0.05)。与升阳益胃汤低剂量组比较,升阳益胃汤中、高剂量组MPO、TGF-β、IL-6水平降低,IL-10水平升高,升阳益胃汤高剂量组DAO水平亦降低(P<0.05)。与升阳益胃汤中剂量组比较,升阳益胃汤高剂量组MPO、IL-6水平降低,IL-10水平升高(P<0.05)。
| 组别 | 鼠数 | MPO | TGF-β | IL-17 | IL-6 | IL-10 | DAO |
|---|---|---|---|---|---|---|---|
| 空白组 | 12 | 68.94±5.61 | 189.60±22.36 | 7.84±1.67 | 82.94±11.45 | 79.16±10.60 | 39.80±7.31 |
| 模型组 | 12 | 98.45±7.65a) | 237.62±22.36a) | 15.15±1.82a) | 101.63±9.06a) | 56.16±8.05a) | 57.69±5.57a) |
| 地塞米松组 | 12 | 79.27±8.53b) | 199.44±15.77b) | 13.39±0.10b) | 92.87±8.13b) | 62.27±5.43b) | 46.16±5.75b) |
| 瑞巴派特组 | 12 | 74.70±7.72b)c) | 195.30±14.46b)c) | 14.23±2.15b) | 91.80±10.93b) | 70.41±10.75b) | 44.86±2.91b)c) |
| 升阳益胃汤低剂量组 | 12 | 92.54±6.74 | 223.56±21.83b)c) | 15.15±1.35 | 100.71±7.77c) | 57.37±6.88c) | 49.61±5.57 |
| 升阳益胃汤中剂量组 | 12 | 90.77±9.10d) | 213.84±29.35b)d) | 14.77±1.58 | 96.41±10.41b)d) | 62.64±5.71b)d) | 48.56±6.43 |
| 升阳益胃汤高剂量组 | 12 | 79.16±11.39b)d)e) | 212.30±21.08b)d) | 14.20±1.34b) | 93.08±7.56b)d)e) | 66.20±8.50b)d)e) | 47.93±2.47b)d) |
2.8 各组大鼠肺组织RORγt、FoxP3 mRNA表达比较
表4示,与空白组比较,模型组大鼠肺组织RORγt mRNA表达升高,FoxP3 mRNA表达降低(P<0.05);与模型组比较,瑞巴派特组、升阳益胃汤高剂量组FoxP3 mRNA表达升高,各给药组RORγt mRNA表达降低(P<0.05);与地塞米松组比较,瑞巴派特组和升阳益胃汤高剂量组FoxP3 mRNA表达升高,瑞巴派特组和升阳益胃汤高、中剂量组RORγt mRNA表达降低(P<0.05);与瑞巴派特组比较,升阳益胃汤低剂量组FoxP3 mRNA表达降低、RORγt mRNA表达升高,升阳益胃汤高剂量组RORγt mRNA表达降低(P<0.05);与升阳益胃汤低剂量组比较,升阳益胃汤中、高剂量组FoxP3 mRNA表达升高,RORγt mRNA表达降低(P<0.05);与升阳益胃汤中剂量组比较,升阳益胃汤高剂量组FoxP3 mRNA表达升高,RORγt mRNA表达降低(P< 0.05)。
| 组别 | 鼠数 | FoxP3/×10-3 | RORγt/×10-3 |
|---|---|---|---|
| 空白组 | 12 | 1.05±0.39 | 1.00±0.09 |
| 模型组 | 12 | 0.22±0.07a) | 3.21±0.96a) |
| 地塞米松组 | 12 | 0.55±0.12 | 1.80±0.29b) |
| 瑞巴派特组 | 12 | 0.72±0.25b)c) | 1.43±0.17b)c) |
| 升阳益胃汤低剂量组 | 12 | 0.39±0.09d) | 1.74±0.25b)d) |
| 升阳益胃汤中剂量组 | 12 | 0.44±0.19e) | 1.49±0.22b)c)e) |
| 升阳益胃汤高剂量组 | 12 | 0.63±0.26b)c)e)f) | 1.25±0.16b)c)d)e)f) |
3 讨论
肺胀是较为复杂的肺系疾病,其虚实夹杂,病情反复,预后不佳,治则常以扶正与祛邪兼顾[3]。《素问·阴阳应象大论篇》曰:“脾生肉,肉生肺。”脾和肺的关系,主要表现为气和水的关系,二者在生理病理上均密不可分[12]。孙思邈《备急千金要方》曰:“凡脾劳病者,补肺气以益之。”李杲认为卫气为元气的组成部分,元气盛则卫气充,故健脾即可补肺,其创立的升阳益胃汤即为治疗肺脾虚证的代表方剂[13-14]。升阳益胃汤扶正与祛邪兼顾,方中陈皮、茯苓、法半夏、炙甘草健脾化痰,黄芪、白术、防风、人参益气固卫、健脾扶正,羌活、独活、柴胡祛风宣肺解表,黄连使里热得清,泽泻使湿邪得导,柴胡加白芍还有升举清阳、疏肝和胃之意。全方寓补于升,气机升降有序,肺气得宣,脾运得健,清阳得升,痰湿得祛,配伍精当巧妙。
研究[15]显示,COPD的发生发展与Th17、Treg介导的免疫失衡密切相关,Th17细胞的分化发育与Treg细胞分化发育呈相互抑制关系。IL-17是Th17细胞的主要效应因子,ROR-γt是其重要的转录因子。IL-17是主要由活化的T细胞产生的致炎细胞因子,可以促进T细胞的激活和刺激上皮细胞、内皮细胞、成纤维细胞产生多种细胞因子如IL-6、IL-8、TGF-β等,从而导致炎症的发生[16]。Treg细胞是维持机体免疫耐受的重要因素之一,Treg细胞主要分泌IL-10等发挥免疫负调控作用,并通过主动调节的方式抑制存在于正常机体内潜在的自身反应性T细胞的活化与增殖,从而调节机体的免疫力,而FoxP3数量减少或功能异常均有可能导致自身免疫病的发生[16]。MPO是一种含血红素的过氧化物酶,主要存在于中性粒细胞中,是中性粒细胞活化的标志,MPO参与了COPD患者肺动脉高压、肺气肿和小气道重塑等病理改变[17]。血清DAO活性水平可作为反映肠黏膜上皮细胞损伤和肠黏膜屏障破坏的指标[18]。
本研究选择对控制炎症有明确效果的地塞米松作为抗炎对照药物,选择对胃肠黏膜有明确修复作用的瑞巴派特作为修复胃肠黏膜对照药物。研究结果显示,瑞巴派特及升阳益胃汤各剂量均能不同程度改善模型大鼠的一般情况,且以升阳益胃汤高剂量效果最好,而地塞米松的改善作用不明显,说明升阳益胃汤和瑞巴派特均可有效改善COPD肺脾气虚大鼠的状态。病理结果显示,模型组大鼠肺、气管及胃、肠组织均有较重损伤,而升阳益胃汤可对上述组织有不同程度的改善效果,且升阳益胃汤高剂量组较中、低剂量组更具有保护和修复胃肠黏膜的作用;地塞米松组对肺组织病理炎性损伤有改善,但对胃肠黏膜无修复作用;瑞巴派特组对胃肠黏膜均有修复作用,但对肺组织病理无明显改善。
本研究结果显示,模型组大鼠外周血Th17水平升高,其分泌的IL-6、IL-17、TGF-β水平及RORγt mRNA表达均升高,而Treg及其分泌的IL-10水平、FoxP3 mRNA表达降低,Th17/Treg值升高,说明大鼠炎症反应较严重,免疫功能失调。而各给药组大鼠外周血Th17、Treg水平及Th17/Treg值均较模型组改善,说明各药物均有调节Th17/Treg平衡的作用,但调节程度不尽相同。升阳益胃汤各剂量组随着药物剂量的增加,下调Th17/Treg值越显著,升阳益胃汤高剂量组在下调Th17/Treg值方面优于瑞巴派特组但不如地塞米松组。升阳益胃汤在降低IL-6及RORγt mRNA表达、升高IL-10及FoxP3 mRNA表达方面亦呈剂量依赖性,说明升阳益胃汤高剂量在改善炎症反应和免疫平衡方面效果最佳。此外,与空白组比较,模型组大鼠MPO、DAO水平升高,说明模型大鼠有肺组织病理损伤和肠黏膜屏障损害。升阳益胃汤高剂量组、地塞米松组及瑞巴派特组DAO及MPO水平均较模型组降低,其中瑞巴派特组降低效果优于地塞米松组,而瑞巴派特组与升阳益胃汤高剂量组两项指标比较差异均无统计学意义,表明各药物均可有效改善肺组织病理及肠黏膜屏障损伤,升阳益胃汤高剂量与瑞巴派特疗效相当。升阳益胃汤低、中剂量组对MPO及DAO的调控不明显,可能与用药剂量太小有关。
综上,升阳益胃汤可综合改善COPD肺脾气虚证大鼠肺、胃、肠炎性损伤,其作用机制可能是通过调节Th17/Treg平衡,从而达到改善气道黏膜、肺部炎症的目的。本研究揭示了升阳益胃汤通过修复胃肠黏膜干预COPD的可能作用机制,为临床使用升阳益胃汤治疗COPD肺脾气虚证提供了实验依据。但本研究采用的干预措施与临床常以中药联合西药吸入疗法控制COPD炎症具有一定差异,因此后期拟进行中西医结合相关临床观察,以提高升阳益胃汤治疗COPD疗效评估的客观性。
Th1/Th17 cytokine profiles are associated with disease severity and exacerbation frequency in COPD patients
[J]. Int J Chron Obstruct Pulmon Dis,2020,15:1287-1299.doi: 10.2147/COPD.S252097.田津,叶佐玉,付丹丹等.升阳益胃汤对慢性阻塞性肺疾病肺脾气虚证模型大鼠组织病理学及血清炎症因子、外周血Th17/Treg平衡的影响[J].中医杂志,2023,64(01):62-70.
TIAN Jin,YE Zuoyu,FU Dandan,et al.Effect of Shengyang Yiwei Decoction (升阳益胃汤) on Histopathology, Serum Inflammatory Factors and Peripheral Blood Th17/Treg Balance in Chronic Obstructive Pulmonary Disease Model Rats with Lung-spleen Qi Deficiency Syndrome[J].Journal of Traditional Chinese Medicine,2023,64(01):62-70.

