基于单靶点的药物研发是当今世界新药研发的重要方法,基于此方法已经研发了一系列上市新药,为现代医药学发展和人类健康作出了重要贡献[1]。随着复杂性疾病逐渐成为威胁人类健康的主要疾病,基于单靶点的药物研发也逐渐暴露出疗效不佳、毒性较大和耐药性的问题[2]。因此,研发针对多靶点、多通路的药物是未来新药研发的重要方向。随着组学技术尤其是转录组学技术的快速发展,针对多基因检测的大规模药物筛选逐渐成为可能,包括连接图谱(connectivity map, CMAP)[3]、L1000研究平台[4]、基于高通量测序的高通量药物筛选(high throughput sequencing-based high throughput screening, HTS2)[5]、基因扰动下的数字RNA测序技术(digital RNA with perturbation of genes-seq, DRUG-seq)[6]等。中药具有多成分、多靶点、多途径的作用特点,故中药新药研发适合与上述技术相结合。
慢性心力衰竭(chronic heart failure,CHF)是不同病因引起器质性心血管病的主要综合征,是临床常见的危重症[7]。近年来,各种新型治疗CHF的化学药和生物药不断研发,但其高死亡率仍未得到根本性逆转,患者5年和10年的生存率分别为56.7%和34.9%[8]。CHF的非药物治疗也有其局限,如心脏移植供体的短缺、心室辅助装置会增加并发症风险等[9]。CHF是中医药治疗的优势病种[10],基于经验的传统中药新药研发模式临床前实践时间过长,作用机制不够清晰,限制了中药新药研发与中医药现代化和国际化。本研究以治疗CHF的中药新药研发为例,在系统阐述其病理机制和中医认识的基础上,利用靶向转录组技术和信号通路富集分析,并结合中医专家经验,借助人工智能技术计算获得创新型治疗CHF的中药方剂,旨在为复杂疾病的中药研发开辟新的有效路径。
1 CHF的病理机制
CHF是由于心脏或血管功能受损引起的交感神经兴奋,肾素-血管紧张素-醛固酮系统持续激活,心脏功能持续受损,并形成心血管病理恶性循环的疾病[11]。此恶性循环一旦形成,心脏射血分数持续降低,血液输出量持续减少,血流速度降低,同时心脏的代偿功能将会激活,导致心肌肥大和心肌纤维化,形成不可逆的心室重塑,导致CHF病情持续发展。同时,心脏功能紊乱会进一步导致肾脏损伤,如肾小管上皮细胞间质转化,形成肾纤维化的病理状态,从而导致水钠的重吸收增加,尿量减少,并引发水肿[12]。
心室重构是CHF发生发展的基本机制,具有心肌细胞肥大、心肌细胞死亡和心肌纤维化三个主要特征[7,13]。在人体心肌组织中,心脏的主要组成包括心肌细胞、心成纤维细胞、内皮细胞和巨噬细胞等,其中心肌细胞占比近30%,心成纤维细胞占比约60%~70%[14]。在机械或生化应激下,心肌细胞发生病理性心肌肥大和心肌细胞死亡,心肌肥大导致心肌细胞功能障碍,心肌细胞死亡导致心肌细胞数量减少[15],这些又会进一步导致心肌成纤维细胞的激活、迁移,并大量分泌细胞外基质蛋白,导致胞外基质沉积,形成心肌纤维化。CHF导致的心输出量降低会引起肾小管间质持续缺血缺氧,各种细胞因子、化学因子及活性氧分子的产生增加,可促进纤维组织增生和细胞外基质紊乱,导致肾间质纤维化和肾单位丢失,进而使患者肾功能损伤[16-17]。有研究[18]通过总结8项共涉及7万余例CHF患者的临床研究发现,合并肾损伤患者的比例平均为45%,估算肾小球滤过率(estimated glomerular filtration rate, eGFR)小于60 ml/(min·1.73 m2),提示肾损伤是重要的合并症。临床研究[19]表明,肾功能受损也会加速CHF的进展,随着肾损伤的增加、eGFR的降低,心源性死亡或因心力衰竭恶化的非计划入院的累积发生率逐步提升。因此,肾功能损伤是CHF的重要病理因素,需要协同调控以达到治疗CHF的目的。
CHF与肾损伤共享许多信号通路,具有大量的心肾交互与串扰作用,包括神经-激素调节、纤维化、细胞凋亡、代谢和营养变化、炎症与免疫反应、应激反应等[17]。传统的CHF西药治疗方案“黄金三角”,即血管紧张素转化酶抑制剂或血管紧张素受体拮抗剂、β受体阻滞剂和醛固酮受体拮抗剂,以及新型的CHF西药治疗“新四联”方案,即β受体阻滞剂、醛固酮受体拮抗剂、血管紧张素受体脑啡肽酶抑制剂和钠葡萄糖共转运蛋白-2抑制剂,均体现了心肾协同调控的作用模式,可见,“心肾同调”是中西医共同认可的治疗CHF的核心手段[20]。
2 中医对CHF的认识
中医学认为,CHF与“喘证”“心水”等相关。“十二五”规划教材《中医内科学》[21]首次在心系疾病中增加了心衰病,与现代医学的急、慢性心力衰竭相对应。中医学对CHF的临床表现记载由来已久,《素问·逆调论篇》曰:“若心气虚衰,可见喘息持续不已”,可见CHF的临床表现之一便是喘证,且与气虚密切相关。《素问·逆调论篇》云:“夫不得卧,卧则喘者,是水气之客也”;“肾者,水藏,主津液,主卧与喘也”。《金匮要略·水气病脉证并治》曰:“心水者,其身重而少气,不得卧,烦而躁,其人阴肿”,可见CHF与水饮密切相关,也体现出其病位在心,与肾脏密切相关。《灵枢·百病始生》曰:“凝血蕴里而不散,津液涩渗。著而不去,而积皆成矣”,提示血瘀是导致水饮内停的重要原因。综上,CHF的基本病机为本虚标实,阳气亏虚,瘀血阻络,水饮内停[22]。在病理状态下,心阳不足,不能温煦推动血液运行,导致阳虚血瘀;心阳不足,日久累及肾阳,导致肾阳不足,气化不利,水液内停,泛逆肌肤,表现为水肿。
中医药在治疗CHF方面具有丰富的临床经验,在延缓病情进展、改善心功能、提高生存质量等方面展现出了明确优势[23-24]。有研究者[10]总结了2006-2016年中医药治疗心血管疾病的循证医学证据,充分证明了中药在改善CHF患者心室重构和心脏功能方面的有效性和安全性。如有研究[25]表明芪苈强心胶囊能显著降低CHF患者的N端脑钠肽前体水平,改善心功能、6分钟步行距离和患者生活质量。因此,基于中医学病机认识,结合中药药理和现代生命科学的最新成果,研发新型的治疗CHF新药具有重要价值。
3 基于靶向转录组的中药方剂研发
传统的中药新药研发模式一般是由临床提供经验方剂,加上长期人用经验使用,再进行新药研发,其临床前研究阶段过长,总体研发历时往往超过10年,且作用机制不十分清晰,这样的新药研发模式已经难以适应新形势下中药新药研发的需求。因此,探索一条新型的中药新药研发路径,缩短临床前研究周期,设计研发安全有效、作用机理清晰的中药新药具有重要的意义。
在此背景下,本课题组提出基于靶向转录组的中药方剂研发思路,该思路是在中医理论指导下,基于现代生命科学信号通路理论,通过靶向转录组测序,利用大数据挖掘、人工智能等手段计算得出的,能逆转患者失调信号通路,具有“多、快、好、省”特点的中药方剂。“多”是指方剂逆转的信号通路多;“快”是指可及性良好,即所需药材能够快速获得;“好”是指疗效好、毒副作用低;“省”是指方剂经济实惠。
靶向转录组筛选技术是基于RNA退火、选择和连接再进行下一代测序(RNA annealing, selection, and ligation with next-generation sequencing, RASL-seq)的药物筛选技术,能够对大规模样本中特定基因集进行检测分析,因此可以特异性地筛选干预疾病相关基因表达的化合物[5]。靶向转录组筛选技术是一项成熟的、可用于高通量药物筛选的方法,可检测特定几千个基因的表达情况,降低了无用序列所占有测序的空间,极大地提高了检测通量和灵敏度,降低了检测成本[26]。蛋白质是细胞内重要的效应子,也是药物治疗的实际靶点,但是由于质谱检测存在样本制备的异质性,以及成本与耗时等问题,较难实现大规模、低成本的基于蛋白质组学或代谢组学的高通量药物筛选[27]。因此,本课题组利用靶向转录组筛选方法建立了大型中药分子功能组学数据库(分子版《本草纲目》平台[28-29]),通过中药提取物处理疾病相关的人源细胞模型,检测细胞内特征基因的表达变化,运用生物信息学分析方法,分析药物的作用基因和信号通路,整合形成了大型中药分子功能组学数据库。
在明确中药作用的信号通路基础上,本课题组提出了采用人工智能技术建立以逆转疾病通路为核心思想的中药智能组方方法。该方法的核心思想是,患者处于病理状态时,其信号通路会出现失调,如果能逆转患者全部失调的信号通路,使其恢复到初始状态,就有可能达到治疗疾病的目的。基于人工智能技术的中药智能组方方法包括:1)基于并行计算的高效穷举算法形成候选复方。利用组合优化算法和递归算法,结合消息传递接口框架,实现候选复方高效生成和并发计算。2)“多、快、好、省”特点的多指标中药方剂评价规则。规则参数包含了候选复方信号通路逆转率,用以筛选调控信号通路多、疗效好的候选复方,药物来源于《中华人民共和国药典》(2020年版)[30](简称《药典》)用以保证可及性,通过《药典》毒性记载和药材价格综合衡量候选复方安全性和经济性。3)通过上述二者结合形成智能高效的通用中药方剂评价软件[31-32],从而实现中药自动组方与筛选。在计算前利用信号通路逆转率对中药单药效果进行排序,提高计算效率,同时,采用并行外部排序算法,加快超大文本的排序处理。
4 基于靶向转录组和专家经验治疗CHF的中药方剂研发过程
基于靶向转录组和专家经验治疗CHF的中药方剂研发过程主要包括三部分:第一,结合中医病机筛选对证中药组成数据库。在中医药理论指导下,针对CHF阳虚、血瘀、痰饮的病机,遵循温阳补气、活血化瘀、化痰利水的基本治则优选核心方剂,再基于穷举算法对核心方剂进行扩展,通过不同排列组合形成海量候选复方[31]。第二,通过靶向转录组检测中药对信号通路的调控作用,以逆转患者失调信号通路为目的,计算候选复方对失调信号通路的逆转率,推荐逆转率排名靠前的中药复方。第三,结合中医专家经验选定方剂和剂量。根据“多、快、好、省”的指导原则对计算方剂加减化裁,优中选优,通过性味平衡分析和专家用药剂量建议最终获得治疗CHF中药方剂。
4.1 结合中医病机筛选对证方药组成数据库
CHF的基本病机为本虚标实,气虚血瘀,日久则心阳亏虚,阳虚水泛,本研究选择真武汤加桂枝汤作为基础方剂,真武汤出自《伤寒论》,具有温阳利水功效。是临床常用治疗CHF的经典方剂[33],真武汤加桂枝汤,则温阳之力更宏。同时,针对CHF主症,选择临床常用的治疗药物,包括温阳补气的黄芪、人参等,活血化瘀的丹参、当归等,化痰利水的猪苓、泽泻等。针对CHF临床症状及兼证,选用陈皮等理气、赤芍等清热、柏子仁等安神、麦冬等滋阴、葶苈子等宣肺平喘。本研究靶向转录组信号通路富集结果提示,黑种草子、珠子参等对CHF相关信号通路具有显著调控作用。上述总计纳入《药典》中92味中药对核心方进行扩展和穷举计算[31]。目前临床常用方剂平均包含13~15味药[34],因此在白术、桂枝、生姜、茯苓、附子、白芍的基础之上,再抽取7~9味药进行排列组合,形成海量(约9.71×1011首)候选复方。
4.2 通过靶向转录组和信号通路分析计算候选复方
研究利用高通量靶向转录组技术检测中药提取物作用于细胞模型后的基因表达。本研究检测了上述98味中药(6味中药来源于真武汤加桂枝汤、92味中药选自《药典》)作用于3种CHF相关细胞(心肌细胞、心成纤维细胞和肾小管上皮细胞)的基因表达谱,并采用基因集富集分析(gene set enrichment analysis, GSEA)方法进行了信号通路富集分析。
CHF患者的失调通路来源于基因表达数据库(gene expression omnibus, GEO)公开的CHF患者心脏及慢性肾病患者肾脏的转录组数据(GSE46224[35]和GSE104954[36]),对转录组数据进行GSEA富集后获得失调信号通路,再筛选出与心肾功能和扶正祛邪相关的信号通路,用于后续的计算。针对心肌细胞,筛选了26条显著变化的失调信号通路;针对心成纤维细胞,筛选了24条失调信号通路;针对肾小管上皮细胞,筛选了32条失调的信号通路。
GSEA算法采用归一化富集分数(normalized enrichment score, NES)体现不同处理对信号通路的调控作用[37],NES的正负衡量信号通路的调控方向,NES为正值,表示上调基因显著富集,NES为负值,表示下调基因显著富集。对于每首候选复方,其调控信号通路的强度用药物总的NES值来表征,即各个组成中药对应信号通路的NES值的加和。针对每条患者失调信号通路,如果患者失调信号通路的NES与模拟候选复方的信号通路的NES值的正负相反,即表示该信号通路被逆转。每首候选复方对CHF的治疗潜力通过信号通路逆转率来衡量[28,38],逆转率等于被逆转的信号通路数除以之前选定的该细胞上与CHF相关的总失调信号通路数[32]。具体公式如下:

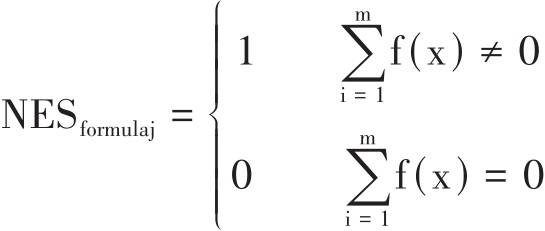
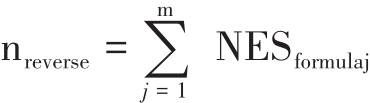
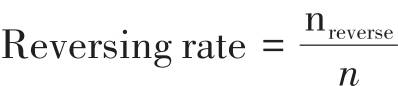
候选方剂逆转率计算公式中,候选方剂中包含m味中药,i表示其中第i味中药。n表示患者失调的信号通路数,也是候选方剂和中药用于计算的信号通路数,j表示第j条信号通路。NESij表示候选方剂第i味中药在第j条信号通路的NES,NESpj表示患者在第j条信号通路的NES值,NESformulaj表示候选方剂在第j条信号通路上是否富集,nreverse表示逆转的信号通路数。Reversing rate表示针对疾病相关信号通路的逆转率。通过靶向转录组和信号通路分析,推荐逆转率排名靠前的组方(附子、白术、桂枝、生姜、白芍、茯苓、黑种草子、珠子参、大枣、旋覆花、泽泻、香橼、鸡血藤),以此为基本方,再根据专家经验进行加减化裁。其对心肌细胞、心成纤维细胞和肾小管上皮细胞的信号通路逆转率分别为92.31%、87.50%和93.75%。
4.3 结合中医专家经验选定方剂
结合中医专家经验对上述13味药组成的基本方进行加减化裁。基于临床经验,保持白术、桂枝、生姜、茯苓、黑种草子、大枣、旋覆花、泽泻、香橼和鸡血藤10味药不变,再进行如下调整:1)考虑方剂的安全性,附子中含有的乌头碱能通过破坏细胞内钙离子的稳态,有致心律失常作用,因此删除了附子[39]。2)考虑CHF的病机和治法,加入黄芪和银杏叶。CHF基本病机是阳虚血瘀、水饮内停,故温阳补气治其本,活血利水治其标。黄芪补气温阳、利水消肿,银杏叶具有活血通络的作用;同时药理研究表明,黄芪[40]、银杏叶[41]具有治疗心肌纤维化、抑制心室重构等作用,故将黄芪、银杏叶2味药加入方剂中。3)讨论对比白芍与赤芍,珠子参与人参对信号通路的调控效果,分别计算其逆转率,目的是获得既能保证较高的信号通路逆转率,又能满足中医药理论可直接用于临床研究的方剂。方剂加入白芍或赤芍,信号通路逆转率相同,但赤芍更长于活血化瘀,故选用赤芍。方剂加入珠子参或人参,两者在心肌细胞和心成纤维细胞上的逆转率相同,但前者在肾小管上皮细胞上的逆转率为93.75%,后者为90.62%,故选用珠子参。
最后,综合考虑方剂的逆转率、毒性、药性和价格,最终得到14味中药组成:黑种草子6 g、黄芪20 g、桂枝9 g、白术10 g、赤芍12 g、鸡血藤10 g、珠子参9 g、银杏叶10g、茯苓15 g、香橼10 g、旋覆花9 g、泽泻10 g、大枣10 g、生姜9 g。根据方剂中的君药黑种草子和黄芪、臣药赤芍、佐药珠子参的名称取首字组合拟定方名为黑黄赤珠饮。方中药物剂量参考《药典》规定和专家经验确定。黑黄赤珠饮组成中包括两味民族药黑种草子和珠子参,这两味药不常用于CHF的治疗,是通过靶向转录组技术挖掘出的创新药物,通过对两味药性味归经、功能主治的深入分析,专家认可了黑种草子和珠子参作为黑黄赤珠饮的组成药物用于CHF治疗。
黑黄赤珠饮具有“多、快、好、省”的特点。“多”体现在黑黄赤珠饮调控的信号通路多。真武汤加桂枝汤原方在三个细胞上的信号通路平均逆转率为67.71%,化裁后组成的黑黄赤珠饮的平均逆转率可达93.96%(见表1)。“快”体现在黑黄赤珠饮的组成中药均来源于《药典》,药用资源丰富,易于获得。“好”体现在黑黄赤珠饮具有明确的作用信号通路,且不含有毒药物。“省”体现在黑黄赤珠饮价格经济实惠,不含人参等贵细药材。另外,中药复方药性对中药新药研发具有重要的指导作用[42]。本研究对黑黄赤珠饮组成中药的整体药性进行了深入分析,结果表明,黑黄赤珠饮性温,为甘、苦、辛味。
| 方剂名称 | 心肌细胞 | 心成纤维细胞 | 肾小管上皮细胞 | 平均 |
|---|---|---|---|---|
| 真武汤加桂枝汤 | 50.00 | 75.00 | 78.13 | 67.71 |
| 黑黄赤珠饮 | 92.31 | 95.83 | 93.75 | 93.96 |
黑黄赤珠饮君药黄芪补气升阳、利水消肿,黑种草子补肾利尿,二者合用可针对CHF主证之气虚、阳虚、水泛,以补气、温阳、利水。臣药桂枝、白术助黄芪以补气温阳,桂枝温阳化气,白术健脾燥湿,得桂枝则温运之力更宏,脾气健运,水湿自除;赤芍、鸡血藤共为臣药,可活血补血,散瘀止痛。茯苓、泽泻为佐药,二者合用使利水渗湿之效倍增,茯苓、桂枝、白术相伍,通阳化气,健脾利水,温而不燥,利而不峻;珠子参、银杏叶为佐药,能活血、祛瘀、止痛,助赤芍、鸡血藤以活血化瘀,珠子参又可补肺养阴,配伍赤芍以敛阴润燥,银杏叶、泽泻还可化浊降脂,增强活血利水之功;香橼、旋覆花亦为佐药,可理气化痰。生姜、大枣共为使药,生姜辛而微温,能助茯苓、桂枝、白术以温中健脾,大枣既能补中益气,又可调和诸药。诸药合用共奏温阳补气、活血化瘀、化痰利水之功。
5 讨论
药物筛选研究从基于单靶点的模式逐渐走向了基于转录组等方法的大数据筛选模式,尤其是CMAP[3]和L1000[4]研究,极大推动了基于高通量测序的药物筛选发展,未来基于此研发的多靶点药物将有助于治疗复杂性疾病。本研究是探索新型中药新药研发路径的一次尝试,通过多学科交叉,结合靶向转录组和专家经验,形成了基于经典名方真武汤加桂枝汤的改良方黑黄赤珠饮,未来也可以形成完全基于运算的智善创新方(即原始创新方)。黑黄赤珠饮是结合中西医学科优势研发的,能在3种CHF相关细胞中协同调控多条信号通路,同时符合中医温阳补气、活血化瘀、化痰利水的治则,有助于改善因阳虚、血瘀、痰饮等病机导致的CHF。
基于转录组的高通量药物筛选为中药新药研发提供了一条可行的路径,但仅基于单组学的方法难以系统全面地解析中药的作用机制,未来可进一步在验证阶段引入蛋白质组学、代谢组学和表型组学等方法,探索基于多组学的中药新药研发路径。目前方法设定CHF涉及的3种细胞对疾病的贡献度一致,因此在提出平均逆转率时使用了算术平均值,未来可考虑设置3种细胞的不同权重来计算候选组方,并在动物模型上验证不同权重候选组方的药效差异。在方剂的药物配比上,本研究是参考《药典》规定和专家经验确定的,未来可以通过设计不同药物配比,在CHF动物模型中,检测血清中关键中药活性成分的药代动力学参数,优化单药剂量,形成方药剂量最佳配比方案。
此外,尽管基于多细胞系的靶向转录组分析可直接推荐安全有效、作用机制清晰的方剂,有望缩短临床前研发时间,但黑黄赤珠饮确切的疗效有待更加完善的随机对照双盲临床试验来加以验证。目前,黑黄赤珠饮配方颗粒的随机对照双盲临床试验研究已经通过中国中医科学院广安门医院伦理委员会的评估与批准(伦理编号:2021-161-KY)正式启动,并在中国临床试验注册中心(Chinese clinical trial registry, ChiCTR)完成了国际注册申报(注册号:ChiCTR2200060028)。
基于靶向转录组的中药方剂研发方法为中医药现代化研究提供了新思路新策略,可系统评价中药治疗疾病的科学内涵、创新中药研发与中药质量控制标准升级等。本研究探索的结合靶向转录组、专家经验和人工智能技术的新药研发路径,也符合中医病证结合的理念。通过靶向转录组和通路富集分析,从微观角度解析中药对CHF关键信号通路的调控作用,针对疾病借助人工智能技术计算候选组方;结合专家经验,从宏观角度针对CHF阳虚、血瘀、水泛的中医证候,进一步优化组方,二者配合,相得益彰。基于已建立的方法论,有望建立一条全新的中药新药研发途径,未来可进一步研发针对糖尿病、冠心病等复杂性疾病、突发传染病的中药新药研发新范式。
Efficacy and safety of traditional Chinese medicine injections for heart failure with reduced ejection fraction: a bayesian network meta-analysis of randomized controlled trials
[J]. Front Pharmacol, 2021, 12: 659707.doi:10.3389/fphar. 2021. 659707.High-throughput strategies for the discovery of anticancer drugs by targeting transcriptional reprogramming
[J]. Front Oncol, 2021, 11: 762023. doi: 10.3389/fonc.2021.762023.乔连生,李军,谢兰等.基于靶向转录组、专家经验和人工智能研发守正创新中药的路径探索——以治疗慢性心力衰竭的中药新药研发为例[J].中医杂志,2023,64(03):217-224.
QIAO Liansheng,LI Jun,XIE Lan,et al.The Exploration of a New Approach for Developing Innovative Chinese Herbal Formulae by Combining Targeted Transcriptome, Expert Experience and Artificial Intelligence: Taking the Development of Anti-chronic Heart Failure Innovative Formula as an Example[J].Journal of Traditional Chinese Medicine,2023,64(03):217-224.

