乙型肝炎是严重危害人类健康的传染病,据统计,截至2017年我国乙型肝炎病毒(hepatitis B virus,HBV)感染者约有7000万例,其中慢性乙型肝炎(chronic hepatitis B,CHB)患者约2000万~3000万例[1]。研究显示,非特异性免疫应答不足是HBV感染的重要因素[2],CHB患者常表现为外周血髓样树突状细胞(myeloid DC, mDC)和浆细胞样树突状细胞(plasmacytoid DC,pDC)数量减少,且mDC成熟障碍,pDC产生干扰素α的能力明显降低,从而导致机体直接清除病毒和诱生HBV特异性T细胞的能力下降[3]。中医学认为,正气不足是CHB发病的内在原因,中医学“正气”所包含的抵御病邪的功能与现代医学免疫系统功能极为相似[4],而免疫耐受期CHB患者均有不同程度的正虚表现[5]。前期研究[6-9]表明,补肾健脾中药可提高CHB患者淋巴细胞功能、促进树突状细胞(dendritic cell,DC)成熟并降低HBV-DNA载量。补肾健脾方由六味地黄丸合四君子汤加黄芪、淫羊藿而成,方中四君子汤为治疗脾气不足的基础方,六味地黄丸为治疗肾阴亏虚的基础方,全方具有健脾益气、滋肾阴温肾阳之效。本实验在前期研究基础上动态观察不同载量HBV对DC亚群的影响,以及补肾健脾方是否可改善HBV对DC各亚群的抑制作用,以期为临床补肾健脾方药治疗乙型肝炎提供实验依据。本研究实验过程符合实验动物福利及伦理相关规范,所用实验动物已经过上海中医药大学动物伦理委员会批准,伦理编号:PZHSUTCM211129019;涉及人生物样本医学研究部分已获得上海中医药大学附属龙华医院伦理委员会批准,批件号:2019LCSY103。
1 材料与方法
1.1 细胞及动物
外周血单个核细胞(PBMC)来自上海中医药大学附属龙华医院招募的6名健康志愿者外周血。HepG 2.2.15细胞株购自上海匹拓生物有限公司(批号:GDC0141)。
6周龄SPF级健康雄性SD大鼠10只,200~250 g,购自上海斯莱克实验动物有限责任公司(合格证编号:20170005054512),饲养于上海中医药大学实验动物中心SPF级动物房,温度:20~26 ℃,湿度:40%~70%,空气洁净度:7级。
1.2 药物
补肾健脾方组成:熟地黄24 g,山药12 g,山萸肉12 g,牡丹皮9 g,泽泻9 g,茯苓9 g,党参9 g,白术9 g,炙甘草6 g,黄芪15 g,淫羊藿9 g。饮片均来自上海中医药大学附属龙华医院药剂科。水煎2次,取汁过滤浓缩为100 ml,其生药浓度为1.23 g/ml。
1.3 主要试剂与仪器
淋巴细胞分离液(货号:LTS1077),天津灏洋华科生物科技有限公司;1640培养基(货号:11875093)、DMEM培养基(货号:11965092),美国赛默飞公司;Hyclone胎牛血清(货号:SH30084),美国Hyclone公司;FITC标记的Lin-1(货号:340546)、PE标记的CD123(货号:554529)、Percp标记的HLA-DR(货号:560652)、APC标记的CD11c流式抗体(货号:340544),美国BD Pharmingen公司。
Millipore Amicon Ultra-15(100.000 MWCO)超滤离心管,德国默克公司;BD FACSVerse™流式细胞仪,美国BD公司;Eppendorf 5804离心机(本实验涉及的离心半径均为14 cm),德国Eppendorf公司。
1.4 PBMC细胞的制备
无菌条件下采集健康志愿者外周血40 ml,PBS等倍稀释,混匀。取50 ml的离心管,加入2倍血液的淋巴细胞分离液,再将混匀的血液缓慢加入,室温1800 r/min离心20 min。离心后离心管内分为三层,上层为血清和PBS液,下层主要为红细胞,中层为淋巴细胞分离液。在上层、中层界面处以单个核细胞为主的灰白色云雾带抽取细胞,加2倍PBS重悬,室温1500 r/min离心10 min取沉淀,2倍PBS重悬,1300 r/min离心5 min取沉淀,1640全培养基重悬备用。
1.5 含药血清的制备
10只SD大鼠按顺序编号,Excel 2010 rand函数生成随机数与之对应,将随机数字从小到大排序,前5个为空白组、后5个为补肾健脾方组。补肾健脾方组大鼠予补肾健脾方24.6 g/(kg·d)灌胃,为人临床等效剂量[10]的2倍;空白组给予等体积生理盐水2 ml/(100 g·d)灌胃。各组大鼠均每日灌胃2次,连续3天。第3天灌胃结束后禁食12 h,次日晨再灌胃1次,补肾健脾方组予补肾健脾方12.3 g/kg灌胃,空白组予1 ml/100 g生理盐水灌胃。末次灌胃后2 h,无菌条件下腹主动脉取血,室温静置2 h后,4 ℃、2500 r/min离心20 min,超净台分离血清。将分离的血清于56 ℃水浴30 min灭活,灭活后过0.22 μm滤膜,-80 ℃冷冻备用。
1.6 HBV病毒液的制备
DMEM全培养基常规培养HepG 2.2.15细胞株,隔日换液,收集培养上清50 ml,置于Millipore Amicon Ultra-15 超滤离心管,4℃、2500 r/min离心20 min,收取离心病毒浓缩液,检测病毒浓缩液HBV载量,调整病毒浓度为1×108 IU/ml。
1.7 分组及给药
1.7.1 低病毒刺激实验
低病毒浓度为1×105IU/孔。将外周血分离的PBMC分为正常组一(1640全培养基2 ml)、低病毒组(1640全培养基2 ml+病毒浓缩液1 μl)、空白血清组一(1640全培养基1.8 ml+病毒浓缩液1 μl+10%空白血清200 μl)、补肾健脾方含药血清组一(1640全培养基1.8 ml+病毒浓缩液1 μl+10%补肾健脾方含药血清200 μl),培养于6孔板,每孔细胞为1×106,每组6个复孔。
1.7.2 高病毒刺激实验
高病毒浓度为1×107IU/孔。将外周血分离的PBMC分为正常组二(1640全培养基2 ml)、高病毒组(1640全培养基1.9 ml+病毒浓缩液100 μl)、空白血清组二(1640全培养基1.7 ml+病毒浓缩液100 μl+10%空白血清200 μl)、补肾健脾方含药血清组二(1640全培养基1.7 ml+病毒浓缩液100 μl+10%补肾健脾方含药血清200 μl),培养于6孔板,每孔细胞为1×106,每组6个复孔。
1.8 DC亚群的检测
干预12、24、36、48 h时检测各组样本中mDC和pDC含量。各组取50 μl加入EP管中调整细胞量为5×105个,分别加入FITC标记的Lin-1抗体5 μl,PE标记的CD123 2.5 μl,Percp标记的HLA-DR、APC标记的CD11c抗体2 μl,避光孵育30 min。30 min后流式仪细胞检测,圈门逻辑为:排除碎片和细胞;圈定Lin弱阳性和阴性细胞;mDC为Lin-,CD11c+,HLA-DR+;pDC为Lin-,CD123+,HLA-DR+。收集细胞后流式细胞仪检测各组mDC和pDC含量。
1.9 统计学方法
采用SPSS 19.0软件。计量资料均呈正态分布,采用均数±标准差(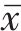
2 结果
2.1 低病毒刺激实验各组细胞不同时间mDC含量比较
表1示,与正常组一同时间比较,低病毒组一2 h时 mDC含量升高、48 h时mDC含量降低(P<0.05),空白血清组一36、48 h时mDC含量降低(P<0.05),补肾健脾方含药血清组一各时间点mDC含量均升高(P<0.05);与低病毒组同时间比较,空白血清组一12 h时mDC含量降低(P<0.05),补肾健脾方含药血清组一各时间点mDC含量均升高(P<0.05);与空白血清组一同时间比较,补肾健脾方含药血清组一各时间点mDC含量均升高(P<0.05)。各组mDC的含量24 h与12 h、48 h与36 h比较差异均无统计学意义(P>0.05);补肾健脾方含药血清组一各时间点之间mDC含量比较差异均无统计学意义(P>0.05),其余各组与本组12 h、24 h比较,36 h、48 h两时间点mDC含量降低(P<0.05)。
| 组别 | 样本数 | 12 h | 24 h | 36 h | 48 h |
|---|---|---|---|---|---|
| 正常组一 | 6 | 0.33±0.07 | 0.36±0.05 | 0.28±0.07d)e) | 0.28±0.07d)e) |
| 低病毒组 | 6 | 0.40±0.04a) | 0.38±0.11 | 0.22±0.04 d)e) | 0.17±0.04 a)d)e) |
| 空白血清组一 | 6 | 0.30±0.05b) | 0.31±0.07 | 0.20±0.04 a)d)e) | 0.16±0.06 a)d)e) |
| 补肾健脾方含药血清组一 | 6 | 0.50±0.04a)b)c) | 0.51±0.07a)b)c) | 0.49±0.07a)b)c) | 0.46±0.05a)b)c) |
2.2 低病毒刺激实验各组细胞不同时间pDC含量比较
表2示,与正常组一同时间比较,低病毒组各时间点pDC含量降低(P<0.05),空白血清组一12、24、48 h时pDC含量降低(P<0.05),补肾健脾方含药血清组一各时间点pDC含量比较差异无统计学意义(P>0.05);与低病毒组同时间比较,空白血清组一各时间点pDC含量比较差异无统计学意义(P>0.05),补肾健脾方含药血清组一各时间点pDC含量均升高(P<0.05);与空白血清组一同时间比较,补肾健脾方含药血清组一各时间点pDC含量均升高(P<0.05)。各组pDC含量24 h与12 h、48 h与36 h比较差异均无统计学意义(P>0.05);与本组12 h、24h比较,正常组一、补肾健脾方含药血清组一36 h、48 h时 pDC含量降低(P<0.05);与本组12 h、24 h比较,低病毒组、空白血清组一48 h 时pDC含量降低(P<0.05);与本组12 h比较,低病毒组36 h 时pDC含量降低(P<0.05)。
| 组别 | 样本数 | 12 h | 24 h | 36 h | 48 h |
|---|---|---|---|---|---|
| 正常组一 | 6 | 0.34±0.08 | 0.35±0.09 | 0.23±0.08d)e) | 0.20±0.05d)e) |
| 低病毒组 | 6 | 0.24±0.05a) | 0.20±0.05a) | 0.14±0.02a)d) | 0.10±0.03a)d)e) |
| 空白血清组一 | 6 | 0.21±0.04a) | 0.19±0.04a) | 0.15±0.05 | 0.11±0.03a)d)e) |
| 补肾健脾方含药血清组一 | 6 | 0.33±0.07b)c) | 0.32±0.06b)c) | 0.25±0.08b)c)d)e) | 0.21±0.06b)c)d)e) |
2.3 高病毒刺激实验各组细胞不同时间mDC含量比较
表3示,与正常组二同时间比较,高病毒组、空白血清组二各时间点mDC含量均降低(P<0.05),补肾健脾方含药血清组二各时间点mDC含量比较差异无统计学意义(P>0.05);与高病毒组同时间比较,空白血清组二各时间点mDC含量比较差异无统计学意义(P>0.05),补肾健脾方含药血清组二各时间点mDC含量均升高(P<0.05);与空白血清组二同时间比较,补肾健脾方含药血清组二各时间点mDC含量均升高(P<0.05)。各组mDC含量24 h与12 h、48 h与36 h比较差异均无统计学意义(P>0.05);与本组24 h比较,正常组二36、48 h 时mDC含量降低(P<0.05);与本组12、24 h比较,高病毒组36、48 h时mDC含量降低(P<0.05);空白血清组二48 h时mDC含量较本组12、24 h降低,36 h时较24 h降低(P<0.05);补肾健脾方含药血清组二36 h时mDC含量较本组12、24 h降低,48 h时较12 h降低(P<0.05)。
| 组别 | 样本数 | 12 h | 24 h | 36 h | 48 h |
|---|---|---|---|---|---|
| 正常组二 | 6 | 0.33±0.07 | 0.36±0.05 | 0.28±0.07e) | 0.28±0.07e) |
| 高病毒组 | 6 | 0.25±0.04 a) | 0.22±0.04 a) | 0.15±0.04 a)d)e) | 0.12±0.03a)d)e) |
| 空白血清组二 | 6 | 0.22±0.03 a) | 0.23±0.05 a) | 0.16±0.05 a)e) | 0.13±0.04a)d)e) |
| 补肾健脾方含药血清组二 | 6 | 0.35±0.07b)c) | 0.32±0.06b)c) | 0.25±0.06b)c)d)e) | 0.27±0.05b)c)d) |
2.4 高病毒刺激实验各组细胞不同时间pDC含量比较
表4示,与正常组二同时间比较,高病毒组、空白血清组二各时间点pDC含量均降低(P<0.05),补肾健脾方含药血清组二各时间点pDC含量比较差异无统计学意义(P>0.05);与高病毒组同时间比较,空白血清组二各时间点pDC含量比较差异无统计学意义(P>0.05),补肾健脾方含药血清组二各时间点pDC含量均升高(P<0.05);与空白血清组二同时间比较,补肾健脾方含药血清组二各时间点pDC含量均升高(P<0.05)。各组pDC含量24 h与12 h、48 h与36 h比较差异均无统计学意义(P>0.05);与本组12、24 h比较,正常组二、补肾健脾方含药血清组二36、48 h时 pDC含量均降低(P<0.05);与本组12 h比较,高病毒组、空白血清组二48 h时pDC含量均降低(P< 0.05)。
| 组别 | 样本数 | 12 h | 24 h | 36 h | 48 h |
|---|---|---|---|---|---|
| 正常组二 | 6 | 0.34±0.08 | 0.35±0.09 | 0.23±0.08d)e) | 0.20±0.05d))e) |
| 高病毒组 | 6 | 0.16±0.05a) | 0.14±0.05a) | 0.12±0.03a) | 0.09±0.03a)d) |
| 空白血清组二 | 6 | 0.17±0.04a) | 0.13±0.04a) | 0.13±0.05a) | 0.10±0.03a)d) |
| 补肾健脾方含药血清组二 | 6 | 0.30±0.05b)c) | 0.30±0.06b)c) | 0.20±0.06b)c)d) e) | 0.18±0.04b)c)d)e) |
2.5 不同载量HBV刺激PBMC细胞后DC亚群含量比较
表5、表6示,高病毒组及低病毒组mDC、pDC含量均随刺激时间的延长呈降低趋势;高病毒组各时间mDC含量均低于同时间点低病毒组(P<0.05),pDC含量仅12 h时低于低病毒组(P<0.05)。高病毒组36、48 h时 mDC含量低于本组12 h、24 h,48 h时 pDC含量低于本组12 h、24 h(P<0.05);低病毒组36、48 h 时mDC、pDC含量均低于本组12 h、24 h,且48 h 时pDC含量低于本组36 h(P<0.05)。
| 组别 | 样本数 | 12 h | 24 h | 36 h | 48 h |
|---|---|---|---|---|---|
| 低病毒组 | 6 | 0.40±0.04 | 0.38±0.11 | 0.22±0.04b)c) | 0.17±0.04b)c) |
| 高病毒组 | 6 | 0.25±0.04 a) | 0.22±0.04a) | 0.15±0.04a)b)c) | 0.12±0.03a)b)c) |
| 组别 | 样本数 | 12 h | 24 h | 36 h | 48 h |
|---|---|---|---|---|---|
| 低病毒组 | 6 | 0.24±0.05 | 0.20±0.05 | 0.14±0.02 b)c) | 0.10±0.03 b)c)d) |
| 高病毒组 | 6 | 0.16±0.05a) | 0.14±0.05 | 0.12±0.03 | 0.09±0.03 b)c) |
3 讨论
CHB是我国的常见病、多发病,中医学将其归为“黄疸”“胁痛”等病症范畴论治。中医学认为,CHB的病因为湿热疫毒之邪侵袭,当人体正气不足无力抗邪时发病,病位在肝,涉及脾、肾;其病机特点为湿热疫毒为标、正气不足为本,属本虚标实、虚实夹杂之证[11]。由于CHB迁延难愈,日久伤正,故治疗时应扶正与祛邪兼顾,调整阴阳、气血、脏腑功能平衡。补肾健脾方中四君子汤加黄芪,健脾益气补益后天之本;六味地黄丸加淫羊藿,滋肾阴温肾阳,养先天之精,全方扶正固本,正切合CHB病机之本。
HBV感染的发病机制较为复杂,迄今尚未完全阐明,其中共价闭合环状DNA(cccDNA)的存在可能是其机制之一。cccDNA是HBV前基因组RNA复制的原始模板,是HBV侵入细胞后在细胞内进行复制的起始步骤,由于cccDNA半衰期较长,难以从体内彻底清除,成为CHB迁延难愈的关键[12]。此外,细胞免疫缺陷也是造成乙型肝炎慢性化的重要原因。DC是人体内功能最强的抗原提呈细胞,在HBV感染者体内的天然免疫和适应性免疫中均发挥着重要的作用[1]。人体外周血DC主要有两个亚群,即mDC和pDC。pDC又称I型干扰素(IFN-I)产生细胞,在病毒感染时,pDC产生IFN-I的能力是其他白细胞的100~1000倍,可分泌大量α干扰素(IFN-α)等细胞因子发挥直接杀伤作用[13-15],并通过IFN-I活化自然杀伤细胞、巨噬细胞等激活天然免疫[16]。mDC相对pDC有更强的抗原呈递能力,能直接激活初始T细胞和B细胞,通过体液和细胞免疫使细胞溶解[17]。HBV及其抗原可造成DC数量异常,HBV感染可阻止DC成熟[18],抑制DC表面CD4、CD80、CD86的表达及成熟 DC生成白细胞介素12(IL-12)和DC对HBV特异性T细胞的活化[19-20],且高载量HBV可以直接导致HBV特异性细胞毒T淋巴细胞呈免疫耐受状态[21]。研究发现,CHB患者外周血DC各亚群存在明显的成熟障碍和功能缺陷,而HBV感染是诱发DC各亚群异常的关键[22-23]。
本研究结果显示,在低病毒刺激实验中,空白血清组一除12 h时mDC含量低于低病毒组外,其余各时间点两组比较差异均无统计学意义,两组各时间点pDC含量比较差异亦无统计学意义,说明空白血清对HBV的刺激无明显作用。与低病毒组及空白血清组一同时间比较,补肾健脾方含药血清组一各时间点mDC、pDC含量均升高,说明补肾健脾方含药血清可有效改善低载量HBV感染对DC亚群的抑制作用。在高病毒刺激实验中,与高病毒组及空白血清组二同时间比较,补肾健脾方含药血清组二各时间点mDC、pDC含量均升高,而高病毒组与空白血清组二各时间点mDC、pDC含量比较差异均无统计学意义,提示补肾健脾方含药血清亦可有效改善高载量HBV感染对DC亚群的抑制作用。同时组内各时间点mDC、pDC含量比较发现,除补肾健脾方含药血清组一mDC含量各时间点无差异外,其余各组36 h、48 h较12 h、24 h均有不同程度降低,提示高、低HBV载量对DC亚群的抑制作用均随时间延长而增强,而补肾健脾方含药血清可有效改善不同载量HBV感染对DC亚群的抑制作用,提高PBMC细胞中mDC、pDC含量,进而增强机体的抗原提呈和干扰素分泌能力,其中以改善低HBV载量对mDC的抑制作用更为明显。
本研究初步验证了补肾健脾方对HBV感染的免疫调节作用,不足之处在于仅探讨了补肾健脾方对DC亚群数量上的影响,而缺乏对mDC、pDC功能以及激活机制的研究,拟于下一步实验中继续进行探索。
Hepatitis B virus persistence and reactivation
[J]. BMJ, 2020,370:Hepatitis B virus cccDNA: Formation, regulation and therapeutic potential
[J]. Antiviral Res, 2020,180:104824.doi: 10.1016/j.antiviral. 2020. 104824.Review of human DC subtypes
[J]. Methods Mol Biol,2010,595:3-20. doi: 10.1007/978-1-60761-421-01.Hepatitis B virus lacks immune activating capacity,but actively inhibits plasmacytoid dendritic cell function
[J]. PLoS One, 2011, 6(1):刘影,张春蕾,单亚维等.补肾健脾方含药血清对乙型肝炎病毒感染后树突状细胞亚群的影响[J].中医杂志,2023,64(01):55-61.
LIU Ying,ZHANG Chunlei,SHAN Yawei,et al.Effect of Bushen Jianpi Formula (补肾健脾方) Drug Containing Serum on Dendritic Cell Subsets after Hepatitis B Virus Infection[J].Journal of Traditional Chinese Medicine,2023,64(01):55-61.

