多囊卵巢综合征(PCOS)是育龄期女性常见的内分泌紊乱综合征,以长期持续无排卵、不孕、高雄激素血症(HA)和胰岛素抵抗(IR)为主要特征,在女性中发病率约为5%~10%[1]。近年来临床研究调查显示,约有50%~70%的PCOS患者伴有IR[2],IR在PCOS的发病机制中发挥着重要作用。IR是PCOS的生殖功能障碍及糖代谢异常的主要病理基础,其导致的代偿性的高胰岛素血症容易破坏卵巢功能,加重PCOS的不孕、闭经等症状,甚至远期还会并发糖尿病、冠心病、高血压等疾病,因此,改善IR对于治疗PCOS尤为重要。现代研究显示,胰岛素后受体信号转导通路障碍是促使PCOS发生IR的主要原因[3-5],也是当前的研究热点之一。目前临床上常用胰岛素增敏剂二甲双胍等治疗PCOS的IR,但西药的不良反应较大,长期治疗不能为患者所接受[6]。近年来中医药防治PCOS已经取得了良好的疗效,中医药具有多靶点、多环节、多途径的特点,可以同时调节PCOS患者内分泌与代谢紊乱,且相对安全[7-9]。由于PCOS患者多存在有肝郁痰阻的临床表现[10],研究表明运用解郁化痰法治疗PCOS具有显著疗效[11]。然而,目前解郁化痰法治疗PCOS的具体作用机制尚不明确。二陈汤源于《太平惠民和剂局方》,是化痰的基础方剂,柴胡疏肝散出自《医学统旨》,为疏肝解郁之代表方剂,二方均分别为临床上用于化痰及疏肝的基础方,临床上常在此二方的基础上进行加减用药治疗,并且疗效显著[12-14]。故本研究以此二方为主,通过单独使用二陈汤、柴胡疏肝散及二方联合运用,从胰岛素信号转导通路探究中医药解郁化痰法治疗PCOS-IR的作用靶点,为中医药防治PCOS-IR提供实验依据。
1 材料
1.1 动物
56只21日龄SPF级雌性SD大鼠,体质量(50±10) g,由上海斯莱克动物有限责任公司提供,许可证号SYXK(闽)2014-0001。饲养于福建中医药大学实验动物中心SPF级屏障系统,饲养环境恒温恒湿,温度(20±2) ℃,湿度40%~60%,12 h周期性光照环境,普通饲料喂养。除实验期外自由饮食、饮水。本实验所有相关动物实验操作均按照动物伦理审查标准严格进行。
1.2 药物及试剂
二陈汤组成根据《太平惠民和剂局方》二陈汤的原方,处方:陈皮15 g,姜半夏15 g,茯苓9 g,炙甘草4.5 g。柴胡疏肝散组成根据《景岳全书》柴胡疏肝散的原方,处方:北柴胡6 g,白芍4.5 g,枳壳4.5 g,川芎4.5 g,醋炒陈皮6 g,香附4.5 g,炙甘草1.5 g。二陈汤+柴胡疏肝散组(合方组)为前述两方合用。上述中药干预采用浓缩液,由福建中医药大学附属第三医院药剂科制备,严格按照2015年版《中国药典》鉴定规范,4 ℃条件下保存备用。二甲双胍片(中美上海施贵宝制药有限公司,0.5 g/片,批号H20023370);脱氢表雄酮(DHEA,上海麦克林生化科技有限公司,批号C10098326);注射用大豆油剂(江西益普生药业有限公司,500 g/瓶,批号20160602);大鼠睾酮(T),雌二醇(E2)酶联免疫吸附测定(ELISA)试剂盒(江苏酶免实业有限公司,批号均为1901R);苏木素-伊红(HE)染色试剂盒(北京索莱宝科技有限公司,批号20180727);逆转录试剂盒,SYBR试剂盒(日本TAKARA公司,批号分别为AI21033A,AI12394A);兔抗胰岛素受体底物(IRS)-1一抗,兔抗IRS-2一抗,兔抗β-肌动蛋白(β-actin)一抗(英国Abcam公司,批号分别为ab52167,ab134101,ab8227);羊抗兔二抗(英国MDL公司,批号MD2141);PCR引物由北京鼎国昌盛生物技术有限责任公司合成,引物序列见表1。
| 引物 | 序列 | 长度/bp |
|---|---|---|
| β-actin | 上游5′-CTCTGTGTGGATTGGTGGCT-3′ | 136 |
| 下游5′-AGCTCAGTAACAGTCCGCCT-3′ | ||
| IRS-1 | 上游5′-CTGCACTCACCCTAGACCCA-3′ | 143 |
| 下游5′-TGACTCCGAAATTCACGCCG-3′ | ||
| IRS-2 | 上游5′-GCATGTTTCCAACCAACGCT-3′ | 197 |
| 下游5′-GAGTGTACTCCATCAGCCCG-3′ |
1.3 仪器
Premium U570型超低温冰箱,5424R型微型冷冻离心机(德国Eppendorf公司);EG1150H型生物组织包埋机,Histocore Pearl型全封闭组织脱水机,RM2245型石蜡切片机(德国Leica公司);SHP-250型生化培养箱(上海精宏实验设备有限公司);QuantStudio6 Flex型实时荧光定量PCR(Real-time PCR)仪(美国Applied Biosystems公司);Nandrop2000型超微量紫外分光光度计(美国Thermo Scientific公司);170-4070型转膜仪,170-3940型半干转印槽,170-3930型垂直电泳系统,Chemi Dox™ XRS+型化学发光凝胶成像仪(美国Bio-Rad公司)。
2 方法
2.1 造模
参照张晓薇等[15]的改良法,选取56只21日龄SPF级SD雌性大鼠,适应性喂养2 d后,按体质量随机分为模型组(44只)和正常组(12只),模型组于颈背部皮下注射DHEA 60 mg·kg-1及注射用大豆油剂0.2 mL,连续20 d。正常组于颈背部皮下注射大豆油剂0.2 mL,连续20 d。于造模第10天后,行2个性周期(10 d)的大鼠阴道脱落细胞涂片,观察大鼠动情周期的变化,并定期观察体质量和摄食情况。于造模结束后,从正常组、模型组各取出4只,麻醉处死,分离卵巢组织,用4%多聚甲醛固定后,行HE染色观察卵巢组织病理学变化,以判定模型建立是否成功。
2.2 模型评价
造模第10天开始观察大鼠阴道脱落细胞变化情况,连续观察2个性周期。正常组阴道涂片按照动情间期、动情前期、动情期、动情后期规律进行;模型组阴道涂片则以黏液和白细胞为主,动情间期延长,失去规律动情周期。于造模结束后,从正常组及模型组各取出4只处死,取卵巢组织,行HE染色观察卵巢形态学变化,正常组镜下可见各级卵泡,成熟卵泡结构完整,有卵丘、卵细胞及放射冠,卵巢颗粒细胞层多为8~9层;模型组镜下可见卵巢呈多囊样变,无成熟卵泡,无卵母细胞及卵丘,卵巢颗粒细胞层多为1~3层,且排列稀疏,少见黄体,证明PCOS模型建立成功。
2.3 分组及给药
将成模后的大鼠随机分为5组,每组8只,分别为模型组、二陈汤组、柴胡疏肝散组、合方组、二甲双胍组,并以正常组(8只)作为对照。造模结束后开始灌胃给药,按照人与动物剂量比例换算,大鼠给药剂量为人剂算的6倍[16-18],二陈汤组给予二陈汤9.135 g·kg-1;柴胡疏肝散组给予柴胡疏肝散6.615 g·kg-1;合方组给予二陈汤+柴胡疏肝散,二方剂量相加9.135 g·kg-1+6.615 g·kg-1;二甲双胍组给予二甲双胍0.158 mg·kg-1,正常组及模型组予等体积灭菌饮用水,每天1次,分别连续干预4周。
2.4 标本取材及处理
于末次给药后,下午8:00开始禁食不禁水。次日称体质量后以10%水合氯醛腹腔注射麻醉,腹主动脉采血,取卵巢、肝脏组织,用预冷的生理盐水洗去组织表面残血,将右侧卵巢组织置于2 mL冻存管内,-80 ℃保存备用,左侧卵巢组织置于4%多聚甲醛中固定,用于HE染色。将肝脏组织切成正方形小块,置于2 mL冻存管内,-80 ℃保存备用。
2.5 ELISA检测大鼠血清中T和E2的含量
大鼠麻醉后腹主动脉取血于促凝管,静置4 h,3 000 r·min-1离心10 min,分离血清。先加样品稀释液40 μL,再加待测样品10 μL,37 ℃孵育30 min,洗涤液洗涤3次,每次5 min。每个反应孔加酶标试剂50 μL,37 ℃孵育30 min,洗涤液洗涤3次,每次5 min。每孔加显色剂A 50 μL,再加显色剂B 50 μL,轻轻震荡混匀,37 ℃避光显色15 min。最后加终止液50 μL,在酶标仪450 nm波长处检测各孔的吸光度A。
2.6 HE染色观察大鼠卵巢组织病理学变化
选取卵巢的最大平面进行石蜡包埋,蜡块分别以4 μm厚度进行连续切片,HE染色并观察,具体染色时间为苏木素染色5 min,伊红染色30 s。
2.7 Real-time PCR检测大鼠肝脏组织中IRS-1和IRS-2 mRNA表达
取肝脏组织进行匀浆,trizol 1 mL提取肝脏组织总RNA,用RNA紫外分光光度计检测肝脏总RNA浓度和纯度,取总RNA逆转录为cDNA。预变性95 ℃ 30 s;PCR反应:95 ℃ 5 s,60 ℃ 31 s,40个循环。以β-actin为内参基因,2-ΔΔCt法计算mRNA表达水平。
2.8 蛋白免疫印迹法(Western blot)检测大鼠肝脏组织中IRS-1和IRS-2蛋白表达
提取肝脏组织中总蛋白,BCA法测定蛋白浓度,根据蛋白浓度,调整上样量,以40 μg/孔的蛋白量进行上样电泳,于湿转槽内将蛋白转印至PVDF膜,经IRS-1,IRS-2一抗(1∶1 500),β-actin一抗(1∶5 000)4 ℃孵育过夜,二抗(1∶2 000)37 ℃孵育1 h,ECL发光,于凝胶成像分析系统中采集PVDF膜发光图像,并测定条带灰度值,以目的蛋白灰度值/内参蛋白灰度值作为统计数据进行统计分析。
2.9 统计学方法
所得数据采用SPSS 21.0统计学软件分析,符合正态分布计量资料均用
3 结果
3.1 对大鼠体质量,T及E2水平变化的影响
用药干预治疗后,各组大鼠体质量无明显差异。与正常组比较,模型组大鼠T水平显著上升,E2水平显著下降(P<0.01);与模型组比较,各给药组T水平显著下降,E2水平显著升高(P<0.01)。见表2。
| 组别 | 剂量/g·kg-1 | 体质量/mg | T/mg·L-1 | E2/mg·L-1 |
|---|---|---|---|---|
| 正常 | - | 269.6±24.6 | 0.31±0.07 | 81.55±5.38 |
| 模型 | - | 263.4±13.7 | 2.50±1.232) | 47.64±6.532) |
| 二陈汤 | 9.135 | 272.6±22.9 | 0.41±0.12 4) | 74.51±3.724) |
| 柴胡疏肝散 | 6.615 | 262.8±22.9 | 0.56±0.204) | 79.48±13.164) |
| 合方 | 15.75 | 268.5±18.8 | 0.45±0.184) | 78.77±9.234) |
| 二甲双胍 | 1.575×10-4 | 265.8±14.6 | 0.43±0.164) | 76.24±5.944) |
3.2 对大鼠卵巢组织病理学的影响
正常组大鼠卵巢组织镜下可见多个黄体及不同发育阶段的卵泡,颗粒细胞呈多层排列,多为8~9层,形态完整。模型组大鼠可见大量的囊状扩张卵泡,囊状卵泡内卵母细胞或放射冠消失,间质细胞增生,卵巢颗粒细胞层数减少,多为2~3层,排列疏松,各级卵泡数目较少。与模型组比较,各用药组可见囊状卵泡数量减少,卵泡颗粒细胞层较模型组增厚,多为5~6层,黄体数量增多,可见有卵丘的成熟卵泡及各级卵泡。见图1。
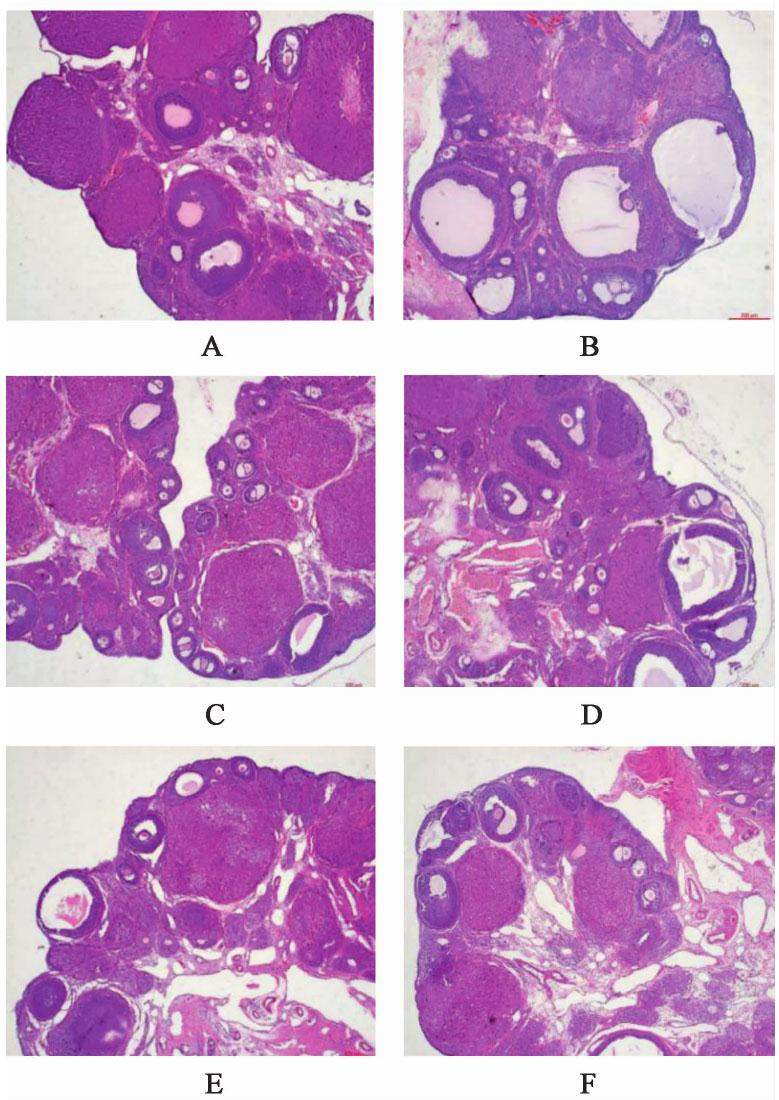
3.3 对大鼠肝脏组织中IRS-1和IRS-2 mRNA表达水平的影响
与正常组比较,模型组大鼠肝脏组织中IRS-1,IRS-2 mRNA表达水平显著下降(P<0.01);与模型组比较,二陈汤组、柴胡疏肝散组及合方组IRS-1 mRNA表达水平明显上升(P<0.05,P<0.01),以二陈汤组上升最为明显;二陈汤组和二甲双胍组IRS-2 mRNA表达水平显著上升(P<0.01),柴胡疏肝散组及合方组IRS-2 mRNA无显著性差异。见表3。
| 组别 | 剂量/g·kg-1 | IRS-1 | IRS-2 |
|---|---|---|---|
| 正常 | - | 1.059±0.224 | 1.033±0.284 |
| 模型 | - | 0.216±0.0592) | 0.384±0.0812) |
| 二陈汤 | 9.135 | 0.875±0.173 4) | 1.193±0.3084) |
| 柴胡疏肝散 | 6.615 | 0.508±0.1374) | 0.841±0.429 |
| 合方 | 15.75 | 0.552±0.1643) | 0.732±0.438 |
| 二甲双胍 | 1.575×10-4 | 0.322±0.0872) | 2.042±0.7984) |
3.4 对大鼠肝脏组织IRS-1及IRS-2蛋白表达水平的影响
与正常组比较,模型组大鼠肝脏组织中IRS-1,IRS-2蛋白表达明显下降(P<0.05,P<0.01);与模型组比较,二陈汤组、二甲双胍组及合方组IRS-1,IRS-2蛋白表达明显上升(P<0.05,P<0.01);柴胡疏肝散组IRS-1蛋白表达明显上升(P<0.05)。见图2,表4。
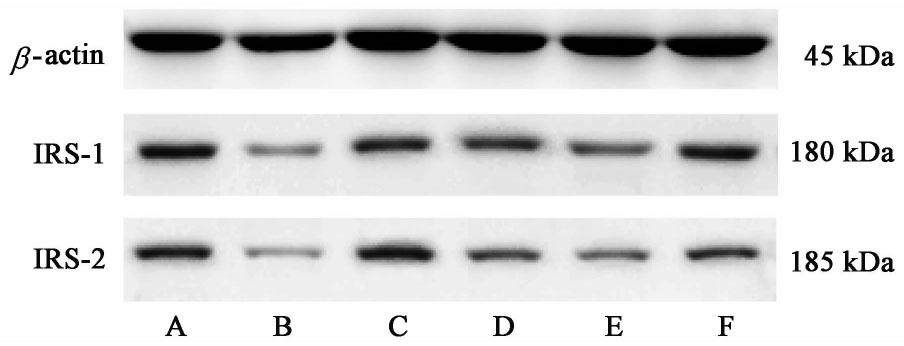
| 组别 | 剂量/g·kg-1 | IRS-1/β-actin | IRS-2/β-actin |
|---|---|---|---|
| 正常 | - | 0.383±0.062 | 0.358±0.150 |
| 模型 | - | 0.224±0.0662) | 0.161±0.0591) |
| 二陈汤 | 9.135 | 0.499±0.1204) | 0.340±0.1423) |
| 柴胡疏肝散 | 6.615 | 0.380±0.1443) | 0.248±0.095 |
| 合方 | 15.75 | 0.372±0.0623) | 0.361±0.1363) |
| 二甲双胍 | 1.575×10-4 | 0.450±0.0734) | 0.404±0.0354) |
4 讨论
近年来,多囊卵巢综合征的患病率呈现逐年升高趋势,已成为危害育龄期妇女生活质量和心理健康的严重疾病之一。研究表明,IR是PCOS的关键环节,在PCOS的发病中占据着重要的地位,是公认导致月经周期异常及不孕的关键原因[19-23]。目前大多数学者认为PCOS发生IR的主要原因是由于胰岛素后受体信号通路障碍所致[24]。而胰岛素受体底物(IRS)作为调节胰岛素信号通路的关健信号分子,对于IR的发生和发展至关重要,其中IRS-1与IRS-2是调节胰岛素信号传导途径的主要船坞蛋白,其蛋白表达和酪氨酸磷酸化异常是发生IR的主要原因[25]。
中医学认为PCOS的发病与肾、脾、肝三脏功能失调有关,由于先天肾气不足,后天脾失健运,肝气郁结,导致气机阻滞,痰湿内生,壅塞胞宫而发病[26]。可见PCOS的病因病机是以肾虚为本,脾虚、肝郁、痰湿为标,虚实夹杂,本虚标实。因此,肝郁和痰湿是PCOS发病的基本病因病机之一,并且中医学认为,肝郁和痰湿也是引起IR发生的主要病理因素[27-32]。
二陈汤源于《太平惠民和剂局方》,是化痰的基础方剂,方中姜半夏、陈皮、茯苓、炙甘草四药合用,共奏燥湿化痰,理气和中之功效。柴胡疏肝散出自《医学统旨》,为疏肝理气之代表方剂,原方由陈皮、北柴胡、川芎、香附、枳壳、白芍、炙甘草等药组成,共奏疏肝理气、活血止痛之功。二者方药分别为治疗痰湿、肝郁的经典代表方剂。因此,本研究通过观察二陈汤、柴胡疏肝散、二陈汤+柴胡疏肝散及二甲双胍对DHEA复制的PCOS模型大鼠的肝脏组织IRS-1,IRS-2 mRNA和蛋白表达的影响,探讨解郁化痰法治疗多囊卵巢综合征的生物学机制。
本实验研究结果显示,模型组大鼠血清T水平显著上升,E2水平明显下降,卵巢组织病理可见大量囊状扩张卵泡,颗粒细胞层较薄,黄体少见,表明PCOS模型建立成功。经过用药治疗后,与模型组比较,各组方药血清T水平明显下降,E2水平明显升高,卵巢组织病理可见囊状扩张卵泡数目减少,颗粒细胞层增厚,可见各级卵泡,故实验结果表明,在PCOS模型大鼠中存在有肝郁痰阻的病理基础。与正常组比较,模型组大鼠的IRS-1,IRS-2 mRNA及蛋白表达显著下调,IRS-1与IRS-2是调节胰岛素信号传导途径的主要船坞蛋白,其蛋白表达变化是发生IR的主要原因。本实验表明二陈汤和柴胡疏肝散均可上调PCOS模型大鼠的IRS-1,IRS-2 mRNA和蛋白表达水平,并且通过实验结果对比发现,二陈汤化痰法调控PCOS模型大鼠的IRS-1,IRS-2 mRNA和蛋白效果较柴胡疏肝散解郁法更为显著,表明了痰是导致PCOS发生IR的主要病理因素。现代研究显示,痰不仅是PCOS发病的关键病因病机,也是PCOS发病过程中的病理产物[33],说明了痰在PCOS发病和后期症状表现中都占据着重要作用。临床调查研究发现,有50%~70%的PCOS患者伴有IR,其发生原因可能是与痰相关。化痰法能够通过调控PCOS模型大鼠肝脏组织的IRS-1,IRS-2 mRNA和蛋白表达水平,从而影响PCOS胰岛素抵抗,改善PCOS症状。现代研究也证实了胰岛素抵抗与痰密切相关[34-35]。中医学认为,胰岛素抵抗发生的机制是由于过食肥甘厚腻,困遏脾土,脾失健运,不能为胃行其津液,水谷不化,湿浊内生,气机阻滞,水谷精微不能正常布散,停滞体内而致。而解郁法也可改善PCOS,但其作用途径可能还通过其他方面实现,有待于进一步深入研究。
综上所述,DHEA诱导的PCOS模型大鼠中存在有肝郁痰阻的病理机制,二陈汤化痰法改善PCOS的IR效果较柴胡疏肝散解郁法更为明显,二陈汤能够通过上调PCOS模型大鼠的肝脏组织IRS-1,IRS-2 mRNA和蛋白表达水平,改善PCOS模型大鼠的胰岛素抵抗,故从以方测证的角度,说明了痰证可能是导致IR发生的主要原因,化痰法治疗PCOS模型大鼠的胰岛素抵抗可能是通过影响胰岛素信号通路的相关信号分子来发挥其作用。

