肺癌是临床常见的恶性肿瘤之一,其发病及死亡率逐年上升[1-2]。肺癌在古代中医文献中没有确切的名称,肺癌可归属为中医肺积、息贲、肺岩等范畴[3]。清燥救肺汤源自于喻嘉言《医门法律》,此方有清燥润肺,益气养阴之功,主治温燥伤肺,气阴两伤。本方配伍巧妙,“宣、清、润、降”并用,补泻兼施,临床疗效明显,故广泛应用于临床[4]。随着中医界对肺癌研究的不断深入,中药治疗肺癌的临床疗效显著,但还存在很大的探索空间[5]。
肿瘤的发生是多种因素综合作用的结果,恶性肿瘤形成是因为肿瘤细胞异常增殖,且凋亡严重减退[6]。因此,抑制肿瘤细胞增殖,促使肿瘤细胞凋亡是当前需要探索的问题。Janus蛋白酪氨酸激酶2/信号转导和转录活化因子3(JAK2/STAT3)作为JAK/STAT通路中的一个重要信号通路,该通路的过度活化与肺癌的发生发展密切相关,能调控多种癌细胞的增殖与凋亡[7]。JAK2的活化不仅与肿瘤的发生发展密切相关,且可参与调控下游STAT3蛋白,二者共同参与细胞增殖和凋亡等过程[8]。STAT3引起癌变的机制主要通过激活细胞周期蛋白D1(Cyclin D1),B淋巴细胞瘤-2(Bcl-2)等靶基因的一些产物表达而实现[9]。STAT3的过度激活可导致细胞异常增殖和恶性转移,通过多种途径促进肺癌细胞增殖和抑制细胞凋亡[10]。而JAK2位于STAT3的上游,JAK2激酶抑制剂AG490,能特定地抑制JAK2,同时也能抑制STAT3的激活,实验研究证明,JAK2激酶抑制剂AG490能有效抑制JAK2/STAT3信号通路,从而使细胞增殖受到抑制[11]。STAT3下游的靶基因,如Bcl-2相关X蛋白(Bax)和Cyclin D1均与细胞增殖和凋亡过程紧密相关[12]。活化的STAT3能促进Bax蛋白的表达,同时对Cyclin D1蛋白的表达起负调控的作用。最新的研究结果表明,癌细胞的增殖和凋亡与JAK2/STAT3信号通路的激活有关[13]。
因此,本论文在前期证实清燥救肺汤能显著抑制肺癌细胞增殖的研究基础上[14],拟建立荷Lewis肺癌小鼠模型,通过观察JAK2/STAT3信号通路及其下游凋亡相关蛋白Bax,Cyclin D1表达的变化,探讨清燥救肺汤的抗肺癌机制。
1 材料
1.1 药物制备
清燥救肺汤:枇杷叶9 g,党参片12 g,生石膏12 g,霜桑叶9 g,阿胶9 g,苦杏仁9 g,麦冬10 g,炙甘草3 g,购于江西省中医院中药房,由江西中医药大学国家工程中心冯育林教授鉴定均为正品,均符合2015年版《中国药典》项下标准。清燥救肺汤详细制备方法参考相关研究[14]。前期的实验结果证实,22,11,5.5,2.75 g·kg-1·d-1清燥救肺汤分别作用于小鼠,清燥救肺汤22 g·kg-1·d-1剂量组没有抑制肿瘤细胞的作用,反而会促进肿瘤细胞增殖,清燥救肺汤11,5.5,2.75 g·kg-1·d-1剂量组有较明显的抑制肿瘤细胞增殖的作用,清燥救肺汤11 g·kg-1·d-1剂量组为人临床剂量换算成小鼠的剂量,故本实验以11 g·kg-1·d-1为高剂量,5.5,2.75 g·kg-1·d-1分别为清燥救肺汤中、低剂量。环磷酰胺(CTX,25 mg·kg-1·d-1)组腹腔注射,隔日1次。
1.2 动物和瘤株
SPF级雄性C57BL/6J小鼠50只,体质量(20±2) g,购于苏州工业园区爱尔麦特科技有限公司,合格证号SCXK(苏)2016-0003;小鼠Lewis肺癌细胞引自ATCC细胞库[14],编号36470TM。本实验经江西中医药大学实验动物伦理委员会审查批准,批号JZLLSC:2017-0030。
1.3 试剂
CTX(江苏恒瑞医药股份有限公司,批号16092525,0.2 g/瓶);乙醇、戊二醛(北京化工厂,批号分别为2018227,20180412);锇酸(上海劲马生物科技有限公司,批号C311498);环氧丙烷(上海桑戈生物科技有限公司,批号E117349);3%乙酸双氧铀染色液(北京生东科技有限公司,批号130452);枸橼酸铅溶液(南京森贝伽生物科技有限公司,批号A93278);磷酸化(p)-JAK2,p-STAT3,Bax,Cyclin D1一抗(美国Affinify公司,批号分别为AF3293,AF3023,AF0120,DF6386);β-肌动蛋白(β-actin)一抗,辣根过氧化物酶(HRP)标记山羊抗兔二抗(美国Proteintech公司,批号分别为20536-1-AP,SA00001-1)。
1.4 仪器
RM2016型切片机(上海徕卡仪器有限公司);TGL-16型高速冷冻离心机(湖南湘仪公司);TECNAI SPIRIT型透射电子显微镜(上海赛默飞仪器有限公司);DMI3000B型倒置显微镜(德国Leica公司);Power Pac TW型电泳仪及转膜仪(美国Bio-Rad公司);WD-9405A型脱色摇床(北京六一仪器厂);XSP-C204型普通光学显微镜(重庆光电仪器有限公司);Fluor Chem M型凝胶成像系统(美国PS公司)。
2 方法
2.1 造模
将小鼠Lewis肺癌细胞置于室温,5%CO2培养箱中进行培养,用10%胎牛血清的DMEM培养基贴壁培养。肺癌细胞取最佳的生长状态,用无菌生理盐水调整密度为5×106个/mL。在小鼠右腋下以每只0.2 mL的接种量行皮下无菌接种[14]。
2.2 小鼠分组和给药方法
50只小鼠,每组10只,随机分为CTX组,模型组,清燥救肺汤高、中、低剂量组。清燥救肺汤高、中、低剂量组造模前2周以规定剂量灌胃给药,每日2次,造模后继续给药2周;模型组,接种24 h,每日用生理盐水0.2 mL灌胃2次;CTX组接种24 h,以规定剂量腹腔注射,隔日1次。接种7 d后,造模小鼠右腋下可触及瘤块,造模过程中无小鼠死亡,即Lewis小鼠动物模型建立成功[15]。造模结束后,处死各组小鼠,取肿瘤组织。
2.3 免疫组化法检测肺癌组织p-JAK2蛋白表达
取肿瘤组织,经多聚甲醛固定,石蜡包埋,切片,不同浓度梯度乙醇逐级脱水,抗原修复,5%牛血清白蛋白封闭后加一抗(1∶100),于4 ℃冰箱孵育过夜,二抗孵育后进行DAB和苏木素染色,脱水、透化、中性树胶封片,以LEICA型倒置显微镜观察并拍照,每张切片在400倍显微镜下,按顺序选取5个视野,用Image-Pro Plus6.0分析,用积分吸光度IA表示蛋白阳性表达相对含量。
2.4 蛋白免疫印迹法(Western blot)检测p-STAT3,Bax,Cyclin D1蛋白表达
取适量肿瘤组织,加入蛋白裂解液,冰上匀浆;4 ℃,12 000 r·min-1离心15 min,取上清,即得总蛋白,BCA法测定蛋白浓度。蛋白上样,聚丙烯酰胺凝胶电泳(SDS-PAGE)分离蛋白,停止电泳后立即将蛋白电转移至PVDF膜上,转膜结束后取出膜,50 g·L-1脱脂奶粉封闭,加入一抗(1∶1 000)4 ℃孵育过夜,洗膜后加入二抗(1∶8 000),室温下孵育1 h,洗膜后进行化学发光,显影,定影。采用Alpha view SA图像分析软件分析蛋白条带灰度值,以β-actin作为内参分析灰度值。
2.5 透射电镜观察肺癌细胞凋亡
取适量肿瘤组织,用1.5%~3%戊二醛固定1~2 h,磷酸盐缓冲液(PBS)洗2次后用1%锇酸固定1~2 h,梯度乙醇脱水;用100%乙醇-环氧丙烷按1∶1在室温下浸泡10 min;Epon812-环氧丙烷按1∶1浸透后放置在真空干燥仪(0.2~0.4 kg·cm-1)2 h,用切片机超薄切片;铀、铅染色,各15,10 min;放置在透射电镜下观察。
2.6 统计学分析
实验采取完全随机设计,以SPSS 20.0软件进行分析,计量资料用
3 结果
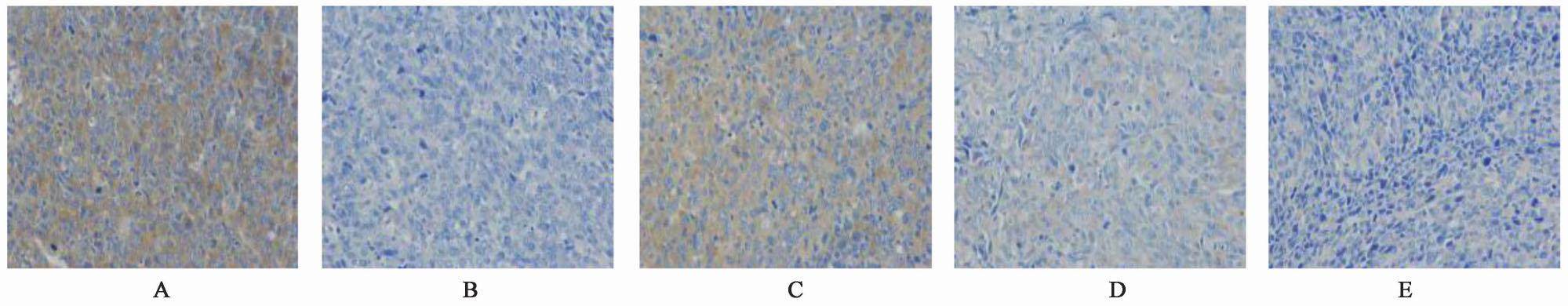
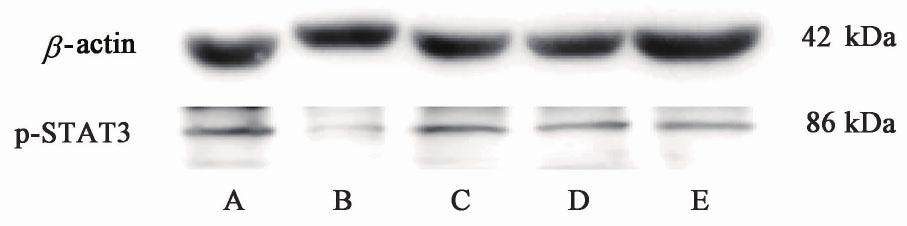
3.1 对荷Lewis小鼠肺癌组织p-JAK2,p-STAT3蛋白表达的影响
与模型组比较,CTX组及清燥救肺汤高、中剂量组肺癌细胞p-JAK2蛋白表达水平明显降低(P<0.05,P<0.01);与CTX组比较,清燥救肺汤低剂量组p-JAK2蛋白表达水平明显升高(P<0.05);与清燥救肺汤高剂量组比较,清燥救肺汤低剂量组p-JAK2蛋白表达水平升高(P<0.05)。与模型组比较,CTX组及清燥救肺汤高、中剂量组p-STAT3蛋白表达水平明显降低(P<0.05,P<0.01);与CTX组比较,清燥救肺汤中、低剂量组p-STAT3蛋白表达水平显著升高(P<0.01);与清燥救肺汤高剂量组比较,清燥救肺汤中、低剂量组p-STAT3蛋白表达水平升高(P<0.01);与清燥救肺汤中剂量组比较,清燥救肺汤低剂量组p-STAT3蛋白表达水平显著升高(P<0.01)。见表1,图1,图2。
| 组别 | 剂量/g·kg-1·d-1 | p-JAK2/β-actin | p-STAT3/β-actin |
|---|---|---|---|
| 模型 | - | 0.208±0.027 | 0.884±0.049 |
| CTX | 0.05 | 0.166±0.0472) | 0.395±0.0602) |
| 清燥救肺汤 | 11 | 0.163±0.0322) | 0.401±0.1001) |
| 5.5 | 0.176±0.0311) | 0.670±0.1421,4,6) | |
| 2.75 | 0.200±0.0323,5) | 0.936±0.0824,6,8) |
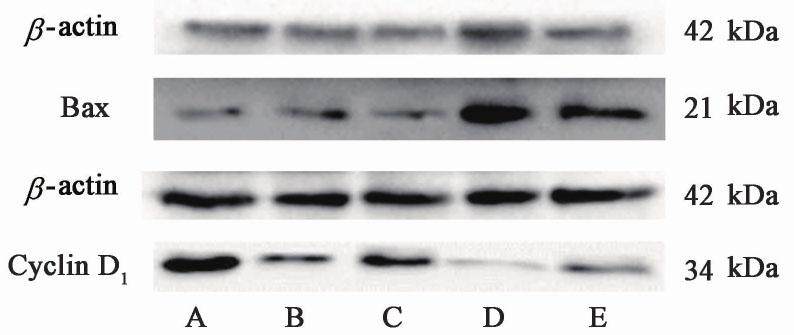
3.2 对荷Lewis小鼠肺癌组织Bax,Cyclin D1蛋白表达的影响
与模型组比较,清燥救肺汤高、中剂量组能显著升高肺癌细胞Bax蛋白表达(P<0.05,P<0.01);与CTX组比较,清燥救肺汤高剂量组Bax蛋白表达升高(P<0.05);与清燥救肺汤高剂量组比较,清燥救肺汤低剂量组Bax蛋白表达显著降低(P<0.01);与中剂量组比较,清燥救肺汤低剂量组Bax蛋白表达降低(P<0.05)。与模型组比较,CTX组及清燥救肺汤高、中剂量组能显著降低肺癌细胞Cyclin D1蛋白表达(P<0.05,P<0.01);与CTX组比较,清燥救肺汤低剂量组Cyclin D1蛋白表达升高(P<0.05)。见表2,图3。
| 组别 | 剂量/g·kg-1·d-1 | Bax/β-actin | Cyclin D1/β-actin |
|---|---|---|---|
| 模型 | - | 0.756±0.133 | 0.969±0.108 |
| CTX | 0.05 | 0.937±0.234 | 0.793±0.0311) |
| 清燥救肺汤 | 11 | 1.279±0.1742,3) | 0.739±0.0362) |
| 5.5 | 1.118±0.0381) | 0.768±0.0551) | |
| 2.75 | 0.821±0.0756,7) | 0.943±0.1263) |
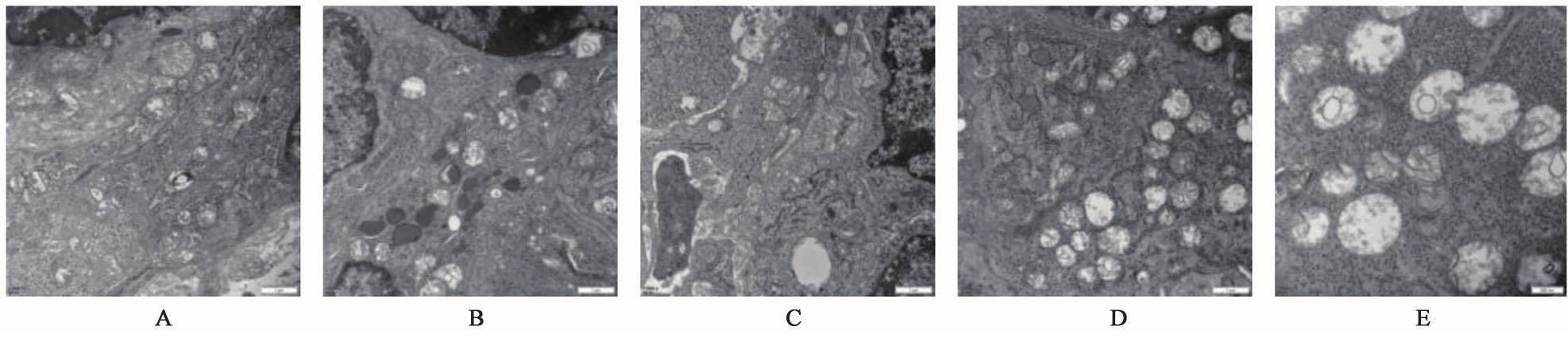
3.3 对肺癌细胞凋亡的影响
模型组细胞核或肿胀或皱缩,部分线粒体肿胀,嵴缩短,胞浆内可见少量空泡;CTX组细胞核或肿胀或皱缩,线粒体肿胀,嵴缩短、减少甚至消失,可见大面积凋亡;清燥救肺汤低剂量组细胞结构较紊乱,细胞核或肿胀或皱缩,细胞器消失,胞浆内少量空泡;清燥救肺汤中剂量组细胞核或肿胀或皱缩,胞浆内空泡,整体凋亡明显,细胞器消失;清燥救肺汤高剂量组细胞结构紊乱,细胞核或肿胀或皱缩,线粒体肿胀,嵴缩短、减少甚至消失,大量细胞凋亡。见图4。
4 讨论
肺癌是严重危害人类健康的恶性肿瘤之一,尽管西医采取多种手段治疗[16],其死亡率仍高居不下,如何提高肺癌的临床疗效是当前亟需解决的重要难题。诸多医家认为燥热伤肺是肺癌的重要病机[17],清燥救肺汤重用霜桑叶清透肺金燥热,为君药;臣以生石膏辛甘而寒,清泄肺热,麦冬养阴润肺。君臣相伍,宣中有清,清中有润。人参片益气生津,合炙甘草以培土生金;苦杏仁、枇杷叶苦降肺气而止咳;阿胶助麦冬养阴润肺,肺得滋润,则治节有权,共为佐药。炙甘草调和诸药,为使。该方主治温燥伤肺,气阴两伤之证,有清燥热、养气阴的功效,对缓解肺癌的燥热症状具有很好的疗效。
细胞凋亡是由基因控制的细胞自主的有序的死亡过程[18],肿瘤的发生是细胞的增加或细胞凋亡的减少,平衡状态被破坏,且大量研究表明,细胞凋亡与肿瘤的发生发展关系密切[19],参与了肿瘤的起始过程,并且可以阻碍肿瘤细胞迅速增长,从而达到一个抑癌的效果[20]。
JAK2/STAT3通路与肿瘤的发生发展密切相关,尤其是STAT3的异常磷酸化在肿瘤的形成中起到了关键作用,活化的STAT3能在胞核中稳定存在,从而使其所调控的下游靶基因表达紊乱,导致细胞的异常增殖[21]。实验研究证明,在多种肿瘤组织中STAT3呈异常表达,过度活化的STAT3对细胞侵袭和增殖等过程起着重要作用,抑制该蛋白可阻断该通路上、下游的致癌因子和致癌基因[22]。
JAK家族共包括4个成员JAK1,JAK2,JAK3,人酪氨酸激酶2(TYK2),其中,JAK2,STAT3的关系最为密切[23]。STAT家族是JAKs下游的一类靶蛋白,JAK2的活化不仅与肿瘤的发生发展密切相关,且可参与调控下游STAT3蛋白,JAK2磷酸化可激活STAT3蛋白使其磷酸化,二者共同参与细胞增殖和凋亡等过程[8]。Bax属于促凋亡蛋白,其促凋亡功能与其结构有关,在细胞凋亡的调控中起重要作用,若Bax的比例增高,则促进细胞凋亡[24];Cyclin D1为细胞周期蛋白,当Cyclin D1的基因结构或功能表达异常时可使细胞周期紊乱,导致细胞无限增殖从而引发肿瘤[25]。
STAT3通过影响肿瘤细胞中C-myc基因(C-myc),Cyclin D1等基因的表达,促使肿瘤细胞持续增殖,干预肿瘤进程[26]。临床研究发现,患者STAT3蛋白高表达或持续被激活,常伴随着C-myc,Cyclin D1基因表达升高[27]。抑制STAT3的活化,可阻断凋亡发生。在大鼠急性肺损伤过程中,其抗凋亡作用可通过STAT3信号通路调控Bax的表达实现[28]。STAT3可通过上调Bax蛋白促进肺癌细胞的凋亡,同时对Cyclin D1蛋白的表达起到负调控的作用。
本研究结果显示,清燥救肺汤可显著降低肺癌细胞JAK2,STAT3蛋白磷酸化水平,并能促进肺癌细胞Bax蛋白表达及显著抑制Cyclin D1蛋白表达。由此可知,清燥救肺汤能显著促进肺癌细胞凋亡,其机制可能与抑制JAK2/STAT3信号通路,上调其下游Bax蛋白表达,下调其下游Cyclin D1蛋白表达有关[29]。

