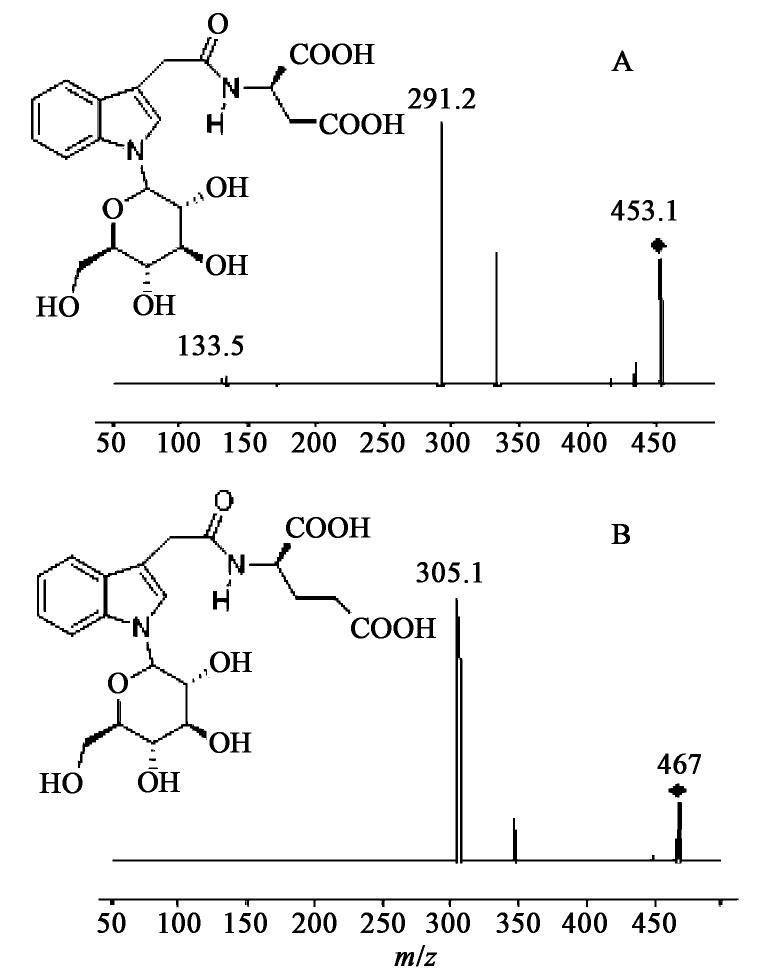
白果为银杏科植物银杏Ginkgo biloba的干燥成熟种子,具有敛肺定喘、止带缩尿的功效,临床上常用于治疗痰多喘咳、带下白浊、遗尿尿频[1]。白果的化学成分主要包括黄酮类、萜类内酯类、白果酸类等[2]。目前,有关白果止咳作用药效物质基础的研究报道较少,仅有文献报道白果中的4′-O-甲基吡哆醇(MPN)有镇咳祛痰的作用[3],但MPN也是白果中主要的一类有毒成分,具有导致中毒死亡的风险[4]。目前尚无其他白果中有止咳作用成分的报道,本课题组前期从白果中分离得到了化合物GK-A,该化合物全名为N-[2-(1-β-D-吡喃葡萄糖基-1H-吲哚-3-基)乙酰基-L-天冬氨酸],见图1(A),并建立了从白果中分离纯化制备GK-A的工艺[5]。前期采用小鼠浓氨水引咳模型,证明GK-A能降低小鼠的咳嗽次数,延长咳嗽的潜伏时间,其止咳作用与阳性药磷酸可待因相当,GK-A是吲哚类生物碱,其结构与磷酸可待因不同,是有很好前景的止咳类新药候选化合物。
从中药及其他天然产物中获得的有效成分是许多新药前体化合物的重要来源[6]。药代动力学在新药研究过程中发挥着重要作用[7],系统阐明GK-A在体内的处置过程是其深入开发研究的重要内容。药物从体内的消除与药物的药效和不良反应关系密切[8],药物进入体内后以多种形式、多种途径排出体外,而尿液排泄和胆汁排泄是药物尤其是极性大的药物从体内排出的重要途径[9]。目前尚无GK-A在体内排泄研究的报道,本研究通过建立UPLC-MS/MS测定大鼠尿液和胆汁中GK-A含量的方法,用于研究灌胃给药后GK-A在大鼠尿液和胆汁中的排泄情况,完善GK-A的体内排泄信息。
1 材料
1290型高效液相色谱仪串联6460型三重四级杆质谱仪(美国安捷伦科技有限公司),TARGIN™ VX-Ⅲ型涡旋混合仪(北京踏锦科技有限公司),5427R型离心机(德国艾本德公司),BS224S-型1/10万电子分析天平(德国赛多利斯公司)。
GK-A与GK-2{内标,N-[2-(1-β-D-吡喃葡萄糖基-1H-吲哚-3-基)乙酰基]-L-谷氨酸,结构式见图1(B)}(实验室自制,纯度均≥98%),水为屈臣氏蒸馏水,甲酸为质谱纯,甲醇、乙腈为色谱纯,其他试剂均为分析纯。
SPF级雄性SD大鼠,体质量(250±20) g,购自斯贝福(北京)生物技术有限公司,合格证号SCXK(京)2014-0006。实验动物饲养在温度(25±2) ℃,相对湿度40%~60%,12 h~12 h循环光照的环境中,保证充足的饲料和饮用水,本实验经中国中医科学院中医基础理论研究所动物伦理委员会批准,伦理编号2017069。
2 方法与结果
2.1 溶液的配制
精密称取GK-A适量,置于100 mL量瓶中,加甲醇定容至刻度,混匀后得质量浓度为0.15 g·L-1的GK-A储备液。精密称取内标适量,置于50 mL量瓶中,加甲醇定容至刻度,混匀后得质量浓度为0.10 g·L-1的内标储备液。
2.2 质控(QC)样品的制备
取GK-A储备液适量,用甲醇稀释,使质量浓度分别为0.24,1.2,12 mg·L-1。分别精密吸取0.24,1.2,12 mg·L-1的GK-A对照品溶液100 μL,于35 ℃氮气吹干后加入空白尿液100 μL,涡旋1 min,即得低(0.24 mg·L-1),中(1.2 mg·L-1),高(12 mg·L-1)3个质量浓度水平的尿液QC样品。分别精密吸取0.24,1.2,12 mg·L-1的对照品溶液50 μL,于35 ℃氮气吹后加入空白胆汁50 μL,涡旋1 min,即得低(0.24 mg·L-1),中(1.2 mg·L-1),高(12 mg·L-1)3个质量浓度水平的胆汁QC样品。
2.3 对照品溶液和内标溶液的制备
精密量取GK-A储备液适量,依次稀释,得质量浓度分别为15.00,7.50,3.00,1.50,0.60,0.30,0.12 mg·L-1的系列对照品溶液。精密量取内标储备液适量,置于25 mL量瓶中,加甲醇稀释至刻度,得质量浓度为8 mg·L-1的内标溶液。
2.4 色谱与质谱条件
2.4.1 色谱条件
Agilent ZORBAX Eclipse Plus C18色谱柱(2.1 mm×50 mm,1.8 μm),流动相0.1%甲酸水溶液(A)-乙腈(B)梯度洗脱(0~1 min,95%A;1~3 min,95%~85%A;3~7.5 min,85%~40%A;7.5~8 min,40%A),流速设定0.2 mL·min-1,柱温35 ℃,进样量0.5 μL。
2.4.2 质谱条件
离子源为电喷雾离子源(ESI),雾化器温度400 ℃,雾化器流速10 L·min-1,喷嘴压力310 266 Pa,鞘气温度350 ℃,鞘气流速11 L·min-1,毛细管电压3.5 kV。GK-A和内标在正模式下测定,选择多重反应监测(MRM)方式测定,二者的定量离子对分别为m/z 453.1~291.1,467.0~305.1,裂解电压分别为85,75 V,碰撞能量分别为9,5 V。
2.5 样品采集与处理
2.5.1 尿液样品的采集与处理[10-11]
取健康雄性SD大鼠6只,禁食不禁水12 h后,按剂量8 mg·kg-1给大鼠灌胃GK-A生理盐水溶液。给药后收集0~6,6~12,12~24,24~36,36~48,48~60,60~72 h时间段的尿液,记录尿液的体积后置于-20 ℃保存。精密吸取大鼠尿液100 μL,加入内标40 μL,加入甲醇(含0.1%甲酸)900 μL,置于涡旋混合器上涡旋混合4 min,于4 ℃,12 000 r·min-1离心10 min,取上清液适量置于自动进样小瓶中进样分析。
2.5.2 胆汁样品的采集与处理[8,12]
取健康雄性SD大鼠6只,禁食不禁水12 h,按剂量10 mg·kg-1给大鼠灌胃GK-A生理盐水溶液,按剂量4 mL·kg-1腹腔注射10%水合氯醛麻醉,待动物麻醉后沿腹中线打开腹腔,实施胆管插管手术。给药后收集0~1,1~2,2~4,4~6,6~8,8~10,10~12,12~24 h时间段的胆汁,记录胆汁体积后置于-20 ℃保存。精密吸取胆汁50 μL,加入内标20 μL,加入甲醇(含0.1%甲酸)550 μL,置于涡旋混合器上涡旋混合4 min,于4 ℃,12 000 r·min-1离心10 min,将上清液转移至5 mL离心管中,37 ℃氮气吹干后加入甲醇(含0.1%甲酸)500 μL复溶,于4 ℃,12 000 r·min-1离心10 min,取上清液适量置于自动进样小瓶中进样分析。
2.6 方法学验证
2.6.1 专属性考察
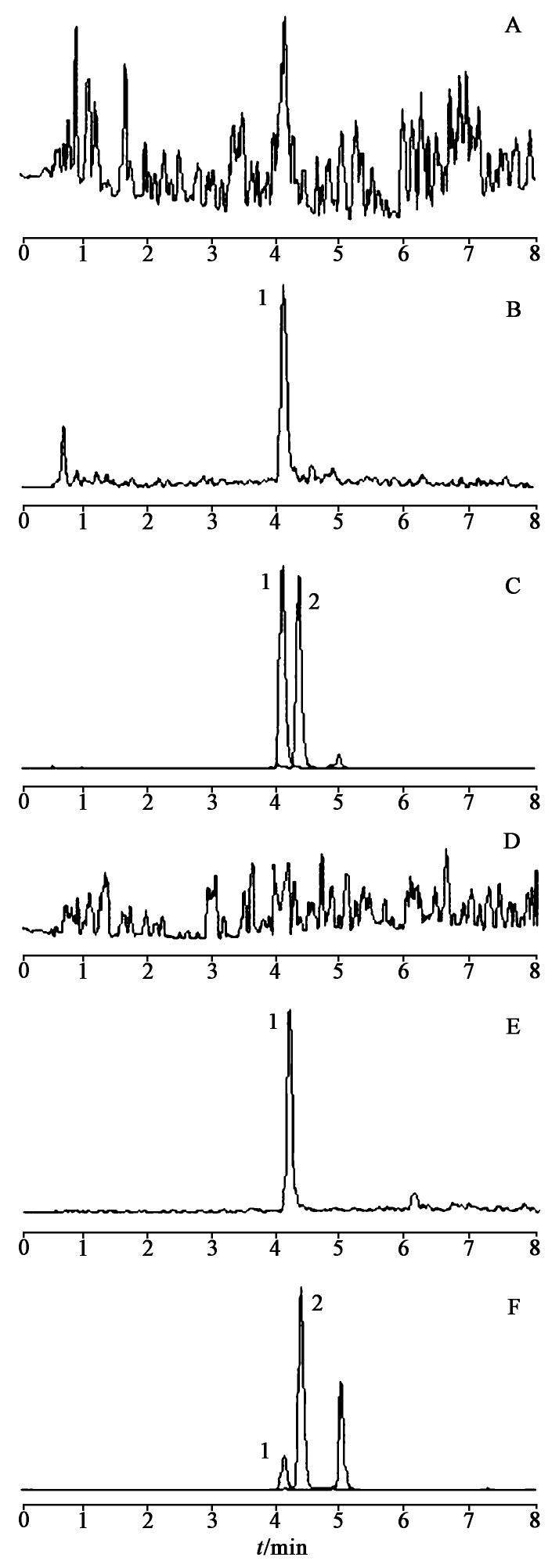
分别取大鼠空白尿液、加入GK-A的空白尿液、给药后的0~6 h的尿液样品适量,按2.5.1项下方法处理后按2.4项下条件进样分析,记录典型的MRM色谱图,见图2。另外,分别取大鼠空白胆汁、加入GK-A的空白胆汁、给药后的4~6 h的胆汁样品适量,按2.5.2项下方法处理后按2.4项下条件分别进样分析,记录典型的MRM色谱图,见图2。结果表明该方法专属性好,尿液和胆汁中内源性物质对GK-A的测定无干扰。
2.6.2 标准曲线与定量下限
精密吸取系列质量浓度的GK-A对照品溶液100 μL,置于5 mL离心管中,于37 ℃氮气吹干,加入空白尿液100 μL,置于涡旋混合器上涡旋2 min,加入内标溶液40 μL,按2.5.1项下方法进行处理,按2.4项下条件进样分析,记录GK-A与内标的峰面积。以待测物与内标峰面积的比值为纵坐标,待测物的质量浓度为横坐标,利用加权最小二乘法(W=1/X2)进行线性回归计算。定量下限(LLOQ)为标准曲线上最低质量浓度。所得标准曲线方程为Y=0.986X+0.019(R2=0.997),LLOQ=0.12 mg·L-1,线性范围0.12~15 mg·L-1。另精密吸取系列质量浓度的GK-A对照品溶液50 μL,置于5 mL离心管中,37 ℃氮气吹干,加入空白胆汁50 μL,置于涡旋混合器上涡旋2 min,加入内标溶液20 μL,按2.5.2项下方法进行处理,按2.4项下条件进样分析,记录GK-A与内标的峰面积。以待测物与内标的峰面积比值为纵坐标,待测物的质量浓度为横坐标,利用加权最小二乘法(W=1/X2)进行线性回归计算。得标准曲线方程为Y=0.6X-0.002(R2=0.998),LLOQ=0.12 mg·L-1,线性范围0.12~15 mg·L-1。
2.6.3 精密度与准确度
分别制备质量浓度为0.12,1.2,12 mg·L-1的尿液(或胆汁)QC样品,每个质量浓度6份,分别按2.5项下方法进行样品处理,按2.4项下条件进样分析,根据标准曲线测定QC样品的质量浓度,连续检测3 d,分别计算日内、日间精密度和准确度,见表1。结果表明尿液样品中日内精密度RSD均≤7.0%,准确度RE处于0.5%~7.7%;日间精密度RSD均≤3.5%,准确度RE处于0~5.3%。胆汁样品中日内精密度RSD均≤5.7%,准确度RE处于-3.2%~13.2%;日间精密度RSD≤3.7%,准确度RE处于-4.4%~12.0%。结果表明建立的测定尿液和胆汁样品中GK-A含量的方法准确度高、精密度好,符合生物样品分析的要求。
| 生物样品 | 质量浓度/mg·L-1 | 日内(n=6) | 日间(n=3) | ||
|---|---|---|---|---|---|
| 精密度RSD | 准确度RE | 精密度RSD | 准确度RE | ||
| 尿液 | 0.24 | 7.0 | 0.5 | 0 | 0 |
| 1.20 | 6.8 | 2.3 | 3.5 | 0 | |
| 12.00 | 3.0 | 7.7 | 2.5 | 5.3 | |
| 胆汁 | 0.24 | 5.1 | -3.2 | 3.5 | -4.2 |
| 1.20 | 5.7 | -0.5 | 3.7 | -4.4 | |
| 12.00 | 4.9 | 13.2 | 1.5 | 12.0 | |
2.6.4 提取回收率和基质效应考察
分别用甲醇制备与尿液(或胆汁)QC样品(0.24,1.2,12 mg·L-1)质量浓度相同的对照品溶液,按2.5项下方法进行处理,按2.4项下条件测定所得分析物的峰面积记为A;分别用空白尿液(或胆汁)处理后的基质溶液制备与质控样品(0.24,1.2,12 mg·L-1)相同质量浓度的样品,按2.5项下方法进行处理,按2.4项下条件进样分析后所得分析物的峰面积记为B;分别取尿液(或胆汁)QC样品(0.24,1.2,12 mg·L-1)按2.5项下方法进行处理,按2.4项下条件进样分析后所得分析物的峰面积记为C。分别计算GK-A在大鼠尿液和胆汁中的回收率和基质效应,其中回收率=C/B×100%,基质效应=B/A×100%,见表2。结果说明所建立的检测方法回收率高(>85%),且无明显的基质效应,符合生物样品分析的要求。
| 生物样品 | 质量浓度/mg·L-1 | 提取回收率 | 基质效应 | ||
|---|---|---|---|---|---|
| 数值 | RSD | 数值 | RSD | ||
| 尿液 | 0.24 | 87.5 | 10.2 | 86.7 | 3.7 |
| 1.20 | 97.7 | 2.5 | 101.8 | 1.8 | |
| 12.00 | 98.2 | 2.7 | 102.5 | 1.9 | |
| 胆汁 | 0.24 | 93.5 | 4.6 | 84.9 | 5.5 |
| 1.20 | 98.2 | 3.5 | 103.8 | 3.1 | |
| 12.00 | 96.9 | 3.1 | 94.3 | 1.3 | |
2.6.5 稳定性考察
分别制备质量浓度为0.24,1.2,12 mg·L-1的尿液(或胆汁)QC样品,每个质量浓度平行6份,按2.5项下方法进行处理后按2.4项下条件进样分析。分别考察尿液(或胆汁)QC样品处理后在室温放置24 h,4 ℃放置24 h,以及反复冻融3次和-20 ℃冻存30 d的稳定性,见表3。结果表明GK-A在上述4种条件下稳定性良好。
| 生物样品 | 质量浓度/mg·L-1 | 室温放置24 h | 4 ℃放置24 h | 冻融3次 | -20 ℃冻存30 d | ||||
|---|---|---|---|---|---|---|---|---|---|
| 测得值/mg·L-1 | RSD/% | 测得值/mg·L-1 | RSD/% | 测得值/mg·L-1 | RSD/% | 测得值/mg·L-1 | RSD/% | ||
| 尿液 | 0.24 | 0.23 | 9.3 | 0.22 | 7.5 | 0.27 | 7.4 | 0.22 | 8.5 |
| 1.20 | 1.16 | 4.2 | 1.14 | 5.6 | 1.35 | 3.7 | 1.09 | 4.1 | |
| 12.00 | 11.85 | 2.4 | 12.08 | 3.0 | 11.91 | 5.3 | 11.55 | 2.8 | |
| 胆汁 | 0.24 | 0.22 | 11.9 | 0.23 | 8.3 | 0.22 | 6.3 | 0.21 | 7.0 |
| 1.20 | 1.09 | 3.9 | 1.15 | 5.1 | 1.08 | 5.8 | 1.03 | 5.2 | |
| 12.00 | 13.15 | 7.7 | 13.04 | 6.6 | 12.50 | 4.9 | 12.48 | 8.5 | |
2.7 GK-A在大鼠尿液和胆汁中的排泄特征分析
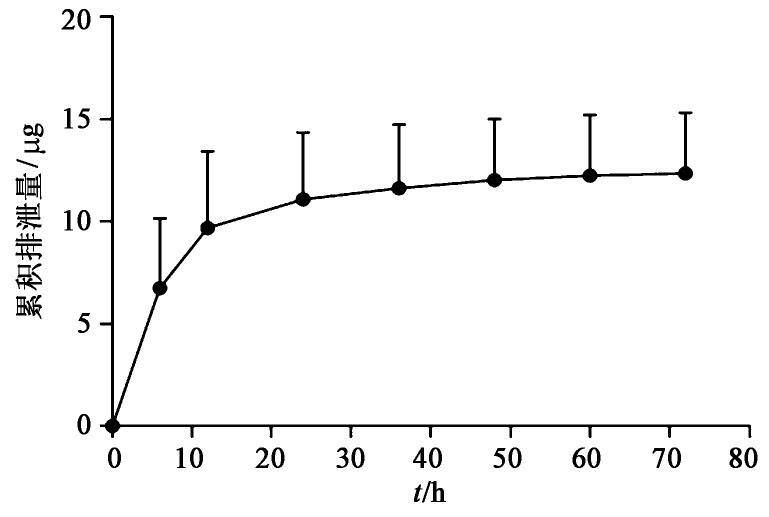
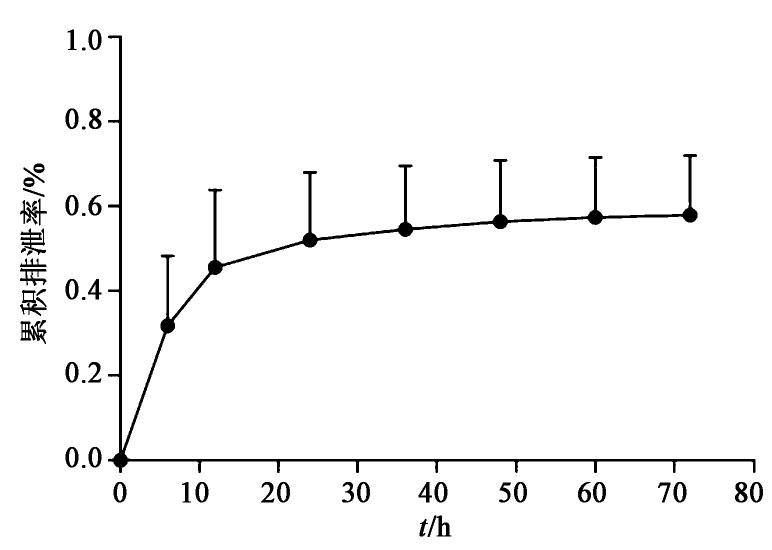
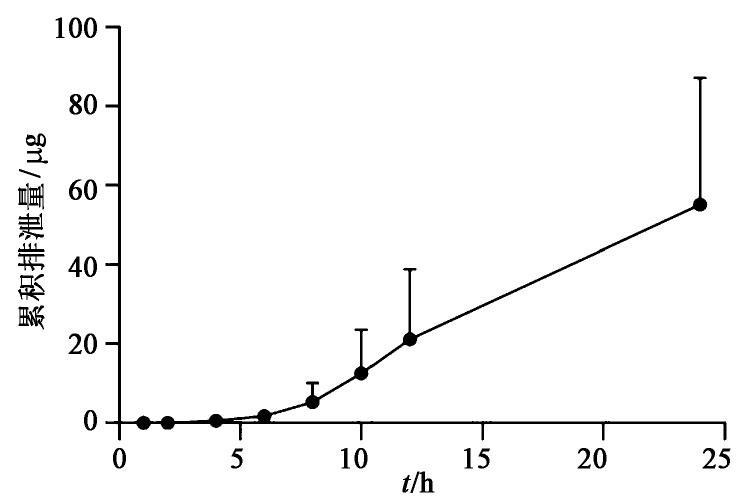
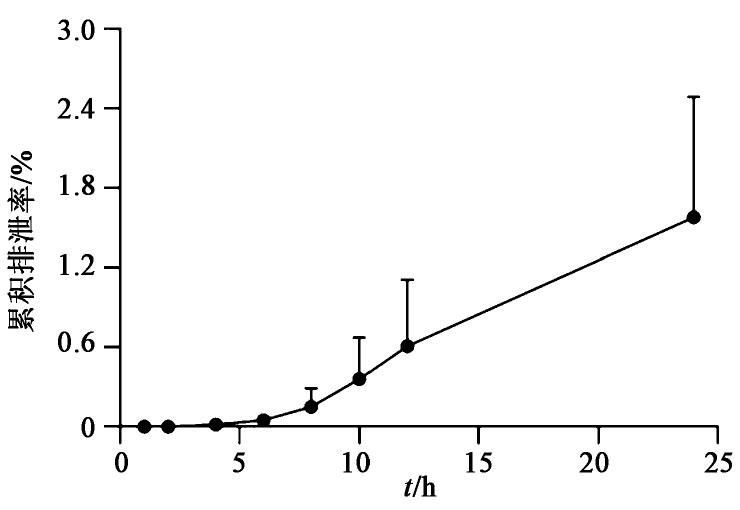
灌胃给予GK-A后分别收集不同时间段大鼠的尿液和胆汁,按2.5项下方法进行处理,按2.4项下条件进样分析,测定各时段尿液和胆汁样品中GK-A的质量浓度,分别计算GK-A在大鼠尿液和胆汁中累积排泄量和累积排泄率。以时间为横坐标,累积排泄量为纵坐标,绘制累积排泄量-时间曲线[12-13];以时间为横坐标,累积排泄率为纵坐标,得累积排泄率-时间曲线;见图3,图4,图5,图6。结果表明灌胃72 h后GK-A在大鼠尿液中的累积排泄量(12.35±2.69) μg,累积排泄率(0.58±0.13)%;在给药24 h后GK-A在大鼠胆汁中的累积排泄量(55.16±29.22) μg,累积排泄率(1.57±0.83)%。提示灌胃给药72 h后GK-A在大鼠尿液中的排泄量已基本达到平衡,其中在0~24 h内GK-A从大鼠尿液中的排泄较快;而在给药24 h后GK-A在胆汁中的排泄量还未达到平衡,其中在6~24 h内GK-A从大鼠胆汁中的排泄较快。由图3,图4,图5,图6可知,GK-A从尿液和胆汁中排泄的速度均较慢,其中的原因还需要进一步研究。
3 讨论
本研究首次建立了UPLC-MS/MS测定大鼠尿液和胆汁中GK-A含量的方法,该方法简便、快速、可靠,并成功应用于研究灌胃给药后GK-A在大鼠尿液和胆汁中的排泄特征。结果表明灌胃给予大鼠GK-A后其原型成分从尿液和胆汁中累积排泄率均<3%,说明GK-A原型经尿液和胆汁排泄的途径不是其主要的消除途径。本研究仅分析了GK-A原型经胆汁和尿液的排泄特征,不足以说明GK-A从体内消除的全部特征,因此,需要进一步研究灌胃给药后GK-A从其他途径排泄的特征。
药物经口服进入体内后会在肠道和肝脏发生代谢反应,因此,阐明GK-A在体内的代谢反应及代谢物的排泄特征,有助于完善GK-A在体内的消除信息。有文献报道,给药剂量[14]和动物性别[15]会影响药物的排泄情况,本研究中仅考察了雄性大鼠单剂量灌胃GK-A后在胆汁和尿液中的排泄特征,后续将进一步研究GK-A的排泄与动物的性别和给药剂量是否有密切的关系,以完善GK-A的体内过程。

